生物醫學工程理論與實踐/生物力學 IV

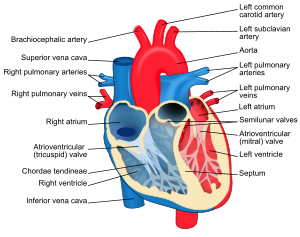
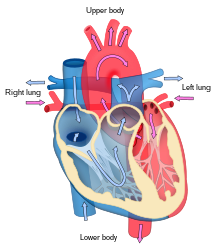
哺乳動物心臟由四個泵室組成:左心房和右心房;左心室和右心室。心房是心臟的兩個上腔室。右心房接受來自上腔靜脈、下腔靜脈和冠狀竇的脫氧血,並將血送入右心室。右心室將血泵入肺動脈乾和肺動脈,進行肺迴圈。左心房接受來自左右肺靜脈的含氧血,並將血泵入左心室,然後透過主動脈泵入全身迴圈系統[1][2]心房的入口沒有瓣膜[3]。在心臟中,心室是心臟的兩個下腔室之一[4]。右心室接受來自右心房的血,並透過肺動脈將其泵入肺部,而左心室接受來自左心房的血,並透過主動脈將其泵入迴圈系統[4]。
表 心肌應力和應變的基本決定因素
| 幾何形狀和結構 | 三維形狀 | 壁厚、曲率、無應力解除安裝參考構型 |
| 組織結構 | 肌纖維結構、結締組織組織、心包、心外膜和心內膜 | |
| 邊界/初始條件 | 壓力 | 充盈壓(前負荷)、動脈壓(後負荷)、直接和間接心室相互作用 |
| 約束條件 | 吸氣和呼氣影響、心包及其附著物引起的約束、瓣膜和纖維瓣環、腱索、大血管、肺 | |
| 材料特性 | 靜息或被動 | 非線性有限彈性、準線性粘彈性、各向異性、雙相多孔彈性 |
| 主動動態 | 啟用順序、肌纖維等長和等張收縮動力學、肌節長度和長度歷史、細胞鈣動力學和代謝能量供應 |
來源:Bronzino, Joseph D. (April 2006). 生物醫學工程手冊,第三版。[CRC 出版社]。p. 54-2。 ISBN 978-0-8493-2124-5.
表 受心肌應力和應變影響的因素
| 直接因素 | 區域性肌肉工作、心肌氧需求和能量學、冠狀動脈血流 |
| 電生理反應 | 動作電位持續時間(QT 間期)、復極化(T 波形態)、興奮性 |
| 發育和形態發生 | 生長速率、心臟迴圈和隔膜形成、瓣膜形成 |
| 易損性 | 缺血、心律失常、細胞脫落 |
| 重塑、修復和適應 | 偏心和同心肥大、纖維化、瘢痕形成 |
| 疾病進展 | 從肥大到衰竭的轉變、心室擴張、梗塞擴張、再灌注反應、動脈瘤形成 |
來源:Bronzino, Joseph D. (April 2006). 生物醫學工程手冊,第三版。[CRC 出版社]。p. 54-2。 ISBN 978-0-8493-2124-5.
膠原蛋白由三螺旋結構組成:兩條相同的鏈 (α1) 和一條在化學成分上略有不同的鏈 (α2)。[5]。膠原纖維的抗拉強度比相同尺寸的鋼絲高[6][7]。迄今為止,已鑑定和描述了 28 種類型的膠原蛋白。五種常見的型別是
- I 型膠原蛋白[8]:這是人體中最豐富的膠原蛋白。它存在於皮膚、肌腱、血管韌帶、器官、骨骼(骨骼有機部分的主要成分)中
- II 型膠原蛋白[9]:它佔軟骨中所有蛋白質的 50% 和關節軟骨中膠原蛋白的 85-90%。II 型膠原蛋白確實會形成原纖維。這種膠原蛋白的原纖維網路會捕獲蛋白多糖聚集體,併為組織提供抗拉強度。
- III 型膠原蛋白[10]:膠原蛋白 α-1(III) 鏈是一種原纖維膠原蛋白,存在於可延展的結締組織中,如皮膚、肺和血管系統,通常與 I 型膠原蛋白一起存在。
- IV 型膠原蛋白:它形成基底膜,即基底膜的由上皮細胞分泌的層。
- V 型膠原蛋白:它存在於細胞表面、頭髮和胎盤中

心肌由心肌細胞、細胞外基質和毛細血管組成。雖然僅佔心臟總蛋白質的 1-4%,但 I 型和 III 型膠原蛋白對於維持心臟的大小和形狀至關重要。膠原基質將心肌細胞、肌絲和毛細血管結合在一起,將力量沿心室壁分佈。心臟細胞外基質主要由原纖維膠原蛋白組成,包括 I 型 (85%) 和 III 型 (11%),由心臟成纖維細胞合成。
膠原蛋白含量、組織、交聯和 I 型與 III 型的比例會隨著年齡的變化而變化,並且在各種疾病狀況下也會發生變化,包括心肌缺血和梗塞、高血壓和肥大[11][12][13]。心肌梗塞後,心肌肌中膠原蛋白的組成會發生變化。在高血壓和心室壓力超負荷期間,它從 40% 增加到 150%。肥大是由於心肌肌中 III 型膠原蛋白的大量增加[14]。原纖維膠原蛋白也是 MI 後瘢痕的主要成分。在心室擴張期間,觀察到膠原蛋白交聯減少,因為成熟的膠原蛋白被新的膠原蛋白取代,而新的膠原蛋白的交聯減少。膠原蛋白的分子間交聯受兩種不同的機制控制。酶促羥賴氨酸吡啶啉交聯的形成由賴氨醯氧化酶催化,賴氨醯氧化酶需要銅作為催化劑。非酶促膠原蛋白交聯,稱為晚期糖基化終產物,由於還原糖的存在而形成[15][16]。由於膠原蛋白對於維持心肌細胞的形狀和排列至關重要,這種弱點會導致心室擴張和收縮功能障礙。

從工程力學角度來看,心室是三維厚壁壓力容器,壁厚和主要曲率在心臟迴圈過程中會發生區域性和時間上的變化。心室壁比心房壁厚,因為它應該產生更高的血壓。正常心臟的心室壁在左心室的赤道和底部最厚,左心室需要將血液泵送到身體的大部分割槽域,而右心室只填充肺部。正常心臟的心室壁在左心室尖端和右心室遊離壁最薄。心室需要將血液泵送到整個身體和肺部的生理負荷遠遠大於心房填充心室的壓力。根據磁共振成像,左心室的平均質量為 143 克±38.4 克,範圍為 87––224 克[17]。右心室的大小與左心室相同,成人約含 85 毫升(3 英制液體盎司;3 美製液體盎司)。


心臟心室具有複雜的 3D 肌纖維結構[18]。肌纖維由肌原纖維組成。肌原纖維由肌動蛋白和肌球蛋白細絲組成,這些細絲以稱為肌節的單元重複出現,肌節是肌肉纖維的基本功能單位。肌節是骨骼肌橫紋外觀和肌肉收縮的原因。在各種哺乳動物的心臟中,雖然心肌細胞相對較短,但它們連線在一起,並以通常由螺旋角和橫向角量化的方向排列[19][20][21][22]。螺旋角表示纖維方向的縱向分量,而橫向角表示纖維方向的橫向分量。測量的橫向螺旋角通常從心內膜下的 +60° 到心外膜下的 -60° 不等,儘管它因測量方法而異。根據心臟壁力學數學模型,認為心肌纖維在心壁內的方向分佈決定了在射血期間整個壁內的應力和肌纖維縮短分佈[23][24][25][26]。
雖然對心室肌纖維結構最可信的結果是透過定量組織學技術獲得的,但擴散張量磁共振成像 (MRI) 已被證明是一種可靠的技術,可以在固定甚至完整的跳動人心臟中無損地估計纖維方向[27][28][29]。根據 David E 等人 (2009 年) 的研究,擴散譜 MRI 纖維束追蹤法 (DSI 纖維束追蹤法) 用於對正常和梗塞的心肌成像。與擴散張量成像不同,DSI 纖維束追蹤法可以解析每個體素中的多個肌纖維群,並且首次生成心肌中存在的準確 3D 纖維束圖[30]。


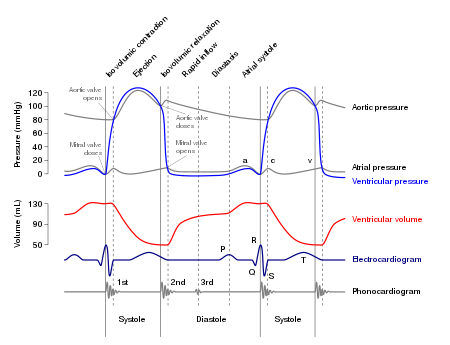
心臟泵最基本力學引數是血壓和血流量,特別是在主要的泵室——心室中。從壁力學角度來看,心室壓力是必不可少的邊界條件。圖中顯示了與左心室壓力和容積有關的心臟迴圈事件。心臟迴圈的階段分為五個步驟:[31]
- 心房收縮:二尖瓣快速開啟,半月瓣關閉。心房收縮並泵血。心室已經從第 5 階段部分充盈,接受最後的約 30% 的血液,最終的休息容積約為 130 毫升。
- 等容收縮:流入血液的減速反轉了瓣膜小葉上的壓力,導致它們關閉,二尖瓣關閉,而半月瓣仍然關閉。心室開始收縮。心室肌最初會略微縮短,但心室壓力會迅速上升(成年人約 50 毫秒)。心室容積不變。
- 心室射血:房室瓣關閉,但半月瓣開啟。左、右心室的壓力超過主動脈壓力(80mmHg)和肺動脈壓力(10mmHg)。射血最初很快,隨著收縮的進行而逐漸減慢。每次心室在靜止狀態下射出的血量為 70-90mL。收縮結束時,每個心室中約有 50mL 的血液。
- 等容舒張:所有瓣膜關閉,因為心室舒張,心室內的壓力降至 120mmHg 以下。一旦心室壓力降至心房壓力以下,房室瓣開啟,舒張結束。心臟將血液泵送到身體的其他部位。
- 心室充盈:房室瓣開啟,半月瓣關閉。心室舒張。心室被動地填充約 70% 的最終容積。隨著心室充盈,充盈速度減慢,房室瓣漂浮向關閉。心房擴張並充滿血液。
心臟週期通常分為兩個階段:收縮期和舒張期。舒張期結束 - 收縮期開始 - 通常定義為二尖瓣快速開啟而半月瓣關閉的時間。

即時左心室 (LV) 壓力-容積曲線有效地展示了心室壓力和容積變化之間的關係。在過去的 20 年中,心室壓力-容積關係得到了廣泛的研究,特別是由佐川等人[32]。心臟週期的等容階段可以是環路的垂直部分,下肢是心室充盈,上段是射血階段。心室充盈壓力的變化(前負荷)沿獨特的舒張末期壓力-容積關係 (EDPVR) 移動舒張末期點,這意味著心室的被動充盈曲線,以及心肌的被動特性。舒張末期點的位置形成舒張末期壓力-容積關係 (ESPVR),它描述了在任何給定 LV 容積下心室所能產生的最大壓力。它在各種條件下呈線性,並且主要獨立於前負荷、後負荷和心率的變化。舒張末期容積 (EDV) 和收縮末期容積 (ESV) 之間的差值是搏出量,即右/左心室在一次收縮中射出的血液量。用數學術語來說,SV = EDV – ESV。
心室壓力-容積環路的面積是心肌對射出的血液所做的搏功的量度。它是搏出量和主動脈或肺動脈平均壓力的乘積(後負荷),取決於考慮的是左心室還是右心室。

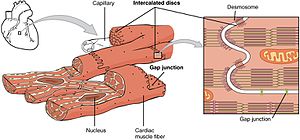

心肌細胞和骨骼肌細胞的收縮機制相似,但並不完全相同。兩種橫紋肌細胞(心肌和骨骼肌)都由稱為肌原纖維的更小單位組成,肌原纖維又由肌節組成。肌節包含重疊的細肌絲和粗肌絲,它們負責肌肉細胞中的力量產生。肌肉產生張力的能力取決於粗肌絲和細肌絲之間的重疊。與骨骼肌相比,心肌需要細胞外鈣離子才能發生收縮。
表 橫紋肌收縮中的基本機械變數。
| 等長張力 ( ) | 肌肉在固定長度下收縮時產生的張力。最大等長張力(對於最大啟用的肌肉)對於骨骼肌來說大約是恆定的,但對於心肌來說,它取決於長度。 |
| 張力 ( ) | 主動產生的張力。通常是等長張力和縮短速度的函式。 ,其中 V 是縮短速度,f(V) 是某種力-速度關係。 |
| 纖維伸長比 ( λ ) | 當前肌節長度除以鬆弛長度。 |
阿奇博爾德·維維安·希爾(1938)[33] 描述了肌肉在恆定負荷下收縮(等張收縮)時的速度和張力之間的關係。 ,其中 是等長張力,V 是速度。a 和 b 是擬合實驗資料的引數。 對於骨骼肌細胞來說是恆定的,但對於心肌細胞來說取決於長度。但是,希爾函式只包括當前速度。
事實上,對於主動收縮肌纖維的詳細數學模型,應該包含以下內容
- 心肌的半最大張力是在 10−6 到 10−5 的細胞內鈣濃度下產生的,M,具體取決於物種和溫度等因素[34]。
- 與肌鈣蛋白 C 結合的鈣濃度,它取決於 和張力 T。
- 可用於橫橋結合的肌動蛋白位點的比例,它取決於與肌鈣蛋白 C 結合的鈣濃度[35]。
- 長度-張力關係和力-速度依賴性。
因此,相對等長收縮張力 最大值可以使用 [36][37] 建模。
Hunter-McCulloch-terKeurs (HMT) 模型[37] 使用以下假設來擬合 Kentish 等人[38] 從大鼠右心室小梁獲得的資料。
其中參考肌節長度 被認為是 2.0 μm。HMT 模型使用標準的 Hill 函式,但將速度 V 替換為所謂的衰減記憶模型,該模型包含有關長度變化歷史的資訊。由於對細胞內鈣的依賴性,HMT 模型與電生理模型的耦合是可以接受的。為了使耦合模型具有現實意義,細胞模型應包含拉伸啟用通道。這允許電生理和肌肉機制之間的雙向耦合,即興奮-收縮耦合和機械-電反饋。HMT 模型僅提供有關單個肌纖維的資訊。肌肉的變形是細胞中產生的主動力的結果,以及組織的彈性特性產生的被動力的結果。為了模擬肌肉組織的變形,需要先進的連續介質力學。
靜息心肌特性:應力和應變
[edit | edit source]
迴圈系統由兩個迴圈(肺迴圈和體迴圈)組成,這兩個迴圈串聯在右心室(RV)和左心室(LV)之間。平衡主要透過 Frank-Starling 機制實現。
心臟瓣膜動力學
[edit | edit source]心臟瓣膜只允許血液沿一個方向流經心臟,允許正向流動並阻止反向流動。通常,人類哺乳動物的心臟中有四個瓣膜。心臟瓣膜的開啟或關閉取決於每側不同的血壓。[39][40][41] 在右心房中,三尖瓣和肺動脈瓣控制著從身體返回肺部的血液流動,以進行氧合。二尖瓣和主動脈瓣調節著從心臟左側流向身體的含氧血液流動。主動脈瓣和肺動脈瓣分別位於心臟左右側主動脈和肺動脈幹或動脈的底部。二尖瓣和三尖瓣分別位於心臟左右側的心房和心室。主動脈瓣和肺動脈瓣在心室收縮的收縮期開啟,並在心室透過開啟的二尖瓣和三尖瓣充盈的舒張期關閉。在等容收縮和舒張期間,所有四個瓣膜都關閉。
半月瓣
[edit | edit source]半月瓣的結構
[edit | edit source]
兩個半月瓣 (SL) 瓣膜,即主動脈瓣和肺動脈瓣,位於主動脈和肺動脈幹或動脈的底部,以及主動脈。這兩個動脈從心室接收血液,它們的半月瓣允許血液被強迫進入動脈,並防止血液從動脈迴流到心室。這些瓣膜沒有腱索,與靜脈中的瓣膜比房室瓣更相似。第二心音是由半月瓣關閉引起的。

主動脈瓣由三個半月瓣或瓣葉組成,包含在一個結締組織套中。瓣葉是一個複雜的、多層結構,厚度為 300~700µm。在橫截面上,瓣葉具有三個不同的層,即纖維層(~45%)、海綿層(~35%)和心室層(~20%)。每個瓣葉都由內皮細胞襯裡,並且在高壓主動脈側有一個緻密的膠原蛋白核心。心室層覆蓋著瓣膜的心室側,由膠原蛋白和彈性蛋白組成。中心部分,稱為海綿層,包括可變的鬆散結締組織和蛋白質。纖維層和心室層內的膠原纖維在無應力狀態下是無序的。當施加應力時,它們主要在周向方向上排列,在徑向方向上彈性蛋白和膠原蛋白的濃度較低[42][43]。肺動脈瓣的解剖結構類似於主動脈瓣,但周圍結構略有不同。研究方法多種多樣。根據病理實驗,主動脈瓣直徑為 23.2 ± 3.3 毫米,而肺動脈瓣直徑測量值為 24.3 ± 3.0 毫米 [44]。但是,根據 M 型超聲心動圖研究,收縮末期主動脈根部直徑為 35 ± 4.2 毫米,舒張末期直徑為 33.7 ± 4.4 毫米[45]。
左心室的收縮期收縮迫使主動脈瓣葉開啟,使含氧血液進入主動脈。當心髒在舒張期休息時,產生的反向壓力梯度會導致主動脈瓣葉關閉。

這些是位於心房和心室之間,防止血液在收縮期從心室迴流到心房的二尖瓣和三尖瓣。二尖瓣和三尖瓣的結構相似,因為兩個瓣膜都由四個主要元素組成:(1)瓣膜環,(2)瓣膜葉,(3)乳頭肌,以及(4)腱索。左側是兩葉的二尖瓣。二尖瓣環是由緻密膠原組織組成的橢圓形環,周圍有肌肉,並附著在二尖瓣葉上。二尖瓣環在心動週期中三維動態地改變大小和形狀。二尖瓣環的正常直徑為 3.1 ± 0.4 釐米,舒張期的周長為 8 到 12 釐米[46][47][48]。在心房收縮結束時,由於左心房圍繞它收縮,它會變小,就像一個括約肌。二尖瓣是一個雙葉瓣,由一個前葉和一個後葉組成。瓣膜組織主要由膠原蛋白加固的內皮和少量橫紋肌細胞、無髓神經纖維、血管組成。瓣膜的前葉和後葉是一塊連續的組織,由連合部隔開。連合部的位置可以透過腱索來識別。兩個葉的總表面積大約是二尖瓣口面積的兩倍;這個額外的表面積有助於二尖瓣環在心動週期中的形狀改變。前葉保護大約三分之二的瓣膜,並分為三個瓣:(1)內側,(2)中央,以及(3)外側瓣[49][50][51][52][53]。雖然前葉佔據了環的大部分,但後葉的表面積更大。這些瓣膜葉透過腱索的作用而不會向左心房突出,腱索是附著在瓣膜後表面上的肌腱。漏瓣可以透過二尖瓣環成形術來矯正。

二尖瓣葉組織可以分為粗糙區和透明區。與二尖瓣不同的是,右側房室環,即三尖瓣,有三個葉:(1)一個前葉,(2)一個後葉,具有數量可變的瓣,以及(3)一個隔葉。三尖瓣比二尖瓣更大,結構也更復雜。
腱索(腱性索)或心絃是將乳頭肌連線到心臟兩個葉的繩索狀肌腱。腱索大約 80% 由膠原蛋白組成,其餘 20% 由彈性蛋白和內皮細胞組成。腱索由一個由膠原蛋白組成的內芯構成,周圍是鬆散的網狀彈性蛋白和膠原蛋白纖維,外面有一層內皮細胞。從每個乳頭肌開始,幾條腱索起源,並分支成邊緣腱索和基底腱索。較薄的邊緣腱索插入葉的遊離邊緣。但較粗的基底腱索在靠近環的更高部位插入葉。邊緣腱索使葉保持靜止,而基底腱索則起到支撐作用[54]。心臟中共有五個乳頭肌,三個在右側三尖瓣中,兩個在左側二尖瓣中。兩個心室的乳頭肌在心室收縮之前不久開始收縮,並在整個過程中保持張力[55][56]。

血管是迴圈系統的一部分,它將血液輸送到人體的各個部位[57]。血管主要有三種類型:動脈,將血液從心臟輸送出去;毛細血管,在血液和組織之間交換水和化學物質;以及靜脈,將血液從毛細血管輸送回心臟[57]。
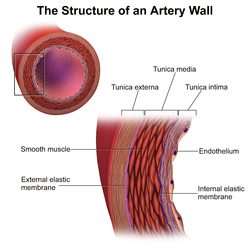
血管由三層組成:內膜、中膜和外膜。
- 內膜(最薄的單層):它由一層內皮細胞組成,並由內彈性膜支撐。它們參與控制血管直徑。
- 中膜(動脈中最厚的一層):它由彈性蛋白、膠原蛋白和平滑肌組成,主要決定血管的彈性特性。
- 外膜:它主要由結締組織組成。它主要由膠原蛋白組成,在動脈中,由外彈性膜支撐。它還包括為血管供血的神經以及較大血管中的營養毛細血管(血管壁血管)。
血管與其他軟生物組織類似,不遵守胡克定律,隨著壓力的增加,會變得更硬。它們還表現出粘彈性特性,如滯後和蠕變。

血液由懸浮在血漿中的血細胞組成。血漿是一種近似牛頓流體,含有 91.5% 的水、7% 的蛋白質和 1.5% 的葡萄糖、礦物質離子、激素、二氧化碳等等[58]。血細胞主要是紅細胞(也稱為紅血球或紅血球)和白細胞,包括白細胞和血小板。在非常小的血管(約 100 μm)中表現出明顯的非牛頓效應。但在較粗的血管中,牛頓假設是可以接受的[59][60]。
動脈中的血流大多是層流,除了近端主動脈和肺動脈以外。血流速度在血管中央最快,在血管壁最慢。通常使用平均速度[61]。
波傳播
[edit | edit source]
血管的粘彈性會影響動脈血流。脈搏波速度 (PWV) 是動脈硬度的一種度量。 [62] [63] 它很容易在人體中進行侵入性和非侵入性測量,並且具有很高的重複性。[64]
莫恩斯-科特韋格方程指出,PWV 與血管壁的增量彈性模量 (Einc) 的平方根成正比,假設血管壁是各向同性的,並且在脈搏壓力下經歷等體積變化,前提是壁厚與血管半徑之比 (h/r) 和血液密度 ρ 保持恆定。[65]
病理
[edit | edit source]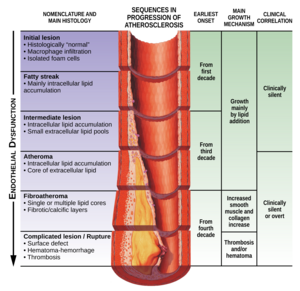
動脈粥樣硬化(也稱為動脈硬化性血管病或ASVD)是一種動脈壁因白細胞(WBC)入侵和積累而變厚的疾病。該病從內膜層的增厚開始,增厚部位與內皮表面剪下應力分佈有關[66]。斑塊(plak)是在動脈內部積聚的物質,由脂肪、膽固醇、鈣和其他血液中發現的物質組成。隨著時間的推移,斑塊會硬化並使動脈變窄。這會限制富含氧氣的血液流向您的器官和身體的其他部位。該疾病對心臟、大腦、手臂、腿部、骨盆和腎臟十分危險。動脈粥樣硬化會導致嚴重的問題,包括心臟病發作、中風,甚至死亡。除了內膜增厚外,動脈壁特性還取決於年齡。
靜脈迴流
[edit | edit source]
靜脈迴流是指血液迴流到心臟的速率。在穩態條件下,靜脈迴流應等於心臟輸出量 (Q),因為心血管系統是一個閉合迴路,在時間上取平均值。否則,血液會積聚在體迴圈或肺迴圈中。迴圈系統由兩個串聯的迴圈(肺迴圈和體迴圈)組成,位於右心室 (RV) 和左心室 (LV) 之間。平衡在很大程度上是透過弗蘭克-斯塔林機制實現的。從血液動力學的角度來看,靜脈迴流 (VR) 到心臟的速率由壓力梯度(靜脈壓 - 右心房壓)和靜脈阻力 (RV) 決定[67]。
心臟輸出量
[edit | edit source]心臟輸出量 (Q 或 或 CO) 是心臟每分鐘泵入迴圈系統的血液量。左心室在一次收縮中輸出的血液量稱為每搏輸出量。每搏輸出量和心率決定心臟輸出量。人類男性平均靜息心臟輸出量 (Q) 為 5.6 L/min,女性為 4.9 L/min。[68]
Q = 每搏輸出量 × 心率
有幾種直接和間接的心臟輸出量測量方法可用。心臟輸出量測量應該準確、精確、與操作員無關、快速響應、無創、連續、易於使用、便宜且安全。目前還沒有這種方法。
菲克的心臟輸出量測量
[edit | edit source]直接菲克氧氣法 [Fick O2]
[edit | edit source]1870 年,阿道夫·菲克描述了一種基於氧氣質量平衡計算心臟輸出量的方法。在這種方法中,測量以下變數:[69]
- VO2,每分鐘消耗的氧氣量,以毫升純氧氣計。這可以用一個封閉的再呼吸回路內的呼吸計進行測量,該回路包含一個二氧化碳吸收器
- Ca,肺靜脈血液中的氧氣濃度(代表氧合血)[70]
- Cv,靜脈導管血液中的氧氣濃度(代表脫氧血)
從這個值來看,
其中 CO = 心臟輸出量,Ca 和 Cv 分別是動脈血和靜脈血的氧氣含量。這使我們能夠說
因此可以計算心輸出量。(Ca – Cv) 也稱為動脈靜脈氧差。[71]
菲克原理可用於遵循亨利定律並透過肺擴散的所有氣體,特別是二氧化碳。NICO(Novametrix Medical Systems Inc. Wallingford, CT, USA)是基於菲克原理為 CO2 研發的心輸出量監測儀,使用間歇性二氧化碳部分再呼吸。菲克方程應用於二氧化碳為
其中 VCO2 是 CO2 產量,CaCO2 和 CvCO2 是血液中的動脈和混合靜脈 CO2 含量。
如今,四種指示劑稀釋技術在市面上可以買到,即肺動脈導管熱稀釋法(透過冷液團注),PAC 連續熱稀釋法,經肺團注熱稀釋法和經肺鋰團注稀釋法。所有這些方法都基於質量平衡
其中 mi 是注入的指示劑量,q(t) 是瞬時血流,c(t) 是濃度隨時間的函式。該方法測量迴圈中不同點染料的濃度,通常來自靜脈注射,然後在下一個取樣點,通常在全身動脈。如果我們假設血流恆定,我們可以找到著名的 Stewart-Hamilton 方程
誤差主要與違反假設、方法實施不準確[72] 和解剖異常[73]有關。
自從 Swan 和 Ganz 在 1970 年[74] 引入配備熱敏電阻的肺動脈導管 (PAC) 以來,熱稀釋法已成為測量患者心輸出量的標準方法。熱稀釋法依賴於熱能守恆定律。以溫度為指示劑,Stewart-Hamilton 方程可以改寫如下
其中 COtd 是熱稀釋法得出的心輸出量,Tb 是注射注入物之前肺動脈中血液的溫度,Ti 是注入物的溫度,∫ΔTb(t)dt 是稀釋曲線下的面積。

Vigilance 系統(Edwards Lifescience,Irvine,CA,USA)利用熱稀釋原理和隨機系統識別技術相結合來測量心輸出量[75]。簡而言之,這些方法涉及從直接輸送到 PAC 右心室部分的 10 釐米熱絲釋放少量熱量。市售的 CCO PAC 使用不同的演算法來分析熱敏電阻在導管尖端測量的熱訊號,從而得出平均心輸出量值。通常,心輸出量的顯示值每 30 秒更新一次,代表前 3 到 6 分鐘的平均心輸出量。因此,當前基於熱訊號的 CCO 方法不應真正被視為連續的即時監測器,而應被視為提供持續的、頻繁更新的心輸出量值的技術。PAC CCO 監測技術在臨床應用中越來越受歡迎。它比團注熱稀釋法心輸出量測量更精確、更可重複,但 CCO 技術的時延需要臨床醫生依賴其他監測變數來檢測急性迴圈變化。由於不需要冷液注射的外接系統,CCO 技術需要更少的護理時間。它可能導致更少的測量誤差、更少的液體超負荷風險和更少的感染風險。這種新方法需要大量的預熱時間,並且可能在熱噪聲較大的環境中效果不佳,例如心臟手術室[75][76]。
這種間歇性熱稀釋技術涉及將一定量的冷液注入右心房入口附近的血流中,並在股動脈中檢測稀釋曲線[77][78][79]。CO 使用與間歇性肺熱稀釋技術類似的 Stewart-Hamilton 方程計算。理論上,經肺熱稀釋技術由於指示劑在肺部不可預測的損失,應該不太準確,但比肺熱稀釋[80][81] 更精確,因為呼吸週期不會影響稀釋曲線。但是,稀釋曲線的信噪比降低了。
鋰稀釋法依賴於靜脈快速注射 1-2 毫升等滲氯化鋰溶液(150-300 毫摩爾)。透過預先放置的外周動脈導管中的鋰感測器測量由此產生的動脈鋰濃度-時間曲線。心輸出量透過 Stewart-Hamilton 方程計算。
其中 Li, dose 是注射的鋰量,∫Δc,li(t)dt 是鋰稀釋曲線的面積,PCV 是紅細胞壓積(計算為血紅蛋白濃度(g dl−1)除以 34)。這種校正措施是必要的,因為鋰只在血漿中稀釋,而不存在於血液的紅細胞和白細胞中。 [82][83]。沒有報道任何副作用。為了使這種技術準確,應該進行三次測量。 [84]。鋰稀釋法被合併到 LiDCO 系統中(LiDCO,倫敦,英國)。該技術未獲準用於體重小於 40 公斤的患者。此外,由於會干擾感測電極,應考慮在接受高劑量神經肌肉阻滯劑的患者中使用鋰稀釋技術。
脈搏波形心輸出量
[edit | edit source]
脈搏壓力(PP)方法測量動脈中的壓力隨時間的變化,以推匯出波形,並使用它來計算心輸出量。但是,從動脈獲得的任何測量值都包含與動脈功能變化相關的壓力變化(順應性、阻抗等)。但是,它易於使用。脈搏波形法估計每搏輸出量基於 Otto Frank 於 1899 年描述的經典 Windkessel 模型。 [85]。目前,有四種商業脈搏波形心輸出量計算器可用:PiCCO、PRAM、LidCO、Vigileo 和 Modelflow。
校準的 PP - PiCCO 系統 [PiCCO] 和 LiDCO 的 pulsco 系統 [LiDCO]
[edit | edit source]PiCCO(PULSION Medical Systems AG,慕尼黑,德國)和 PulseCO(LiDCO Ltd,倫敦,英國)透過分析動脈 PP 波形來進行連續 Q 測量。在這兩種情況下,都需要一種獨立的技術來校準連續 Q 分析,因為動脈 PP 分析無法解釋未測量的變數,例如血管床順應性的變化。患者體位、治療或狀況發生變化後,需要重新校準。
PiCCO 演算法總結在以下方程中。
其中 COpi 是心輸出量,K 是校準因子,HR 是心率,P 是動脈血壓,∫P(t)dt 是壓力曲線收縮期部分的面積,SVR 是外周阻力,Cp 是依賴壓力的動脈順應性,dP/dt 表示壓力波形的形狀。校準因子 (K) 透過肺動脈熱稀釋法測量。在 SVR 發生重大變化後和定期(≥1 小時)間隔時,需要重新校準。 [86][87][88]。需要進行侵入性導管插入。對於 PiCCO 裝置,可以使用橈動脈和股動脈途徑。 [89]。
在 LiDCO 的情況下,獨立的校準技術是使用 Stewart-Hamilton 原理的氯化鋰稀釋法。氯化鋰稀釋法使用外周靜脈到外周動脈導管。與 PiCCO 一樣,在 Q 發生變化後,需要頻繁校準。最近的資料表明,每 8 小時重新校準一次,或者在發生重大血流動力學變化時重新校準一次。 [84]。
壓力記錄分析法 [PRAM]
[edit | edit source]PRAM(Vytech Health,帕多瓦,義大利)是 Wesselings cZ 演算法的改進版本。 [90]。PRAM 透過分析從動脈導管(橈動脈或股動脈通路)獲得的壓力波形來估計 CO。搏出量 (SV) 與動脈壓力波的舒張期部分的面積除以特徵阻抗 (Z) 成正比。比例因子透過與獨立的 SV 測量值(例如間歇熱稀釋法)進行校準獲得。與其他方法相比,PRAM 不依賴於校準或人口統計資料。使用 PRAM,Z 從整個心搏的壓力曲線形態資料中獲得,計算為 Z = (P/t) × K(t)。因此,搏出量 (SV) 遵循以下公式:
其中 A 是壓力曲線收縮期部分的面積,P/t 是每個心搏的壓力 (P) 隨時間 (t) 變化的壓力波形的解析描述,K(t) 是與主動脈橫截面積的瞬時加速度成反比的因子。使用 PRAM,計算每個搏動的心搏量,然後透過將 SV 與相同搏動的心率相乘來推匯出每搏心輸出量。CO 被描述為 12 個搏動的平均值。由於 PRAM 的內部校準是根據壓力曲線的形態推匯出來的,因此 PRAM 在穩定狀態下沒有達到所考慮的標準方法。 [92] 以及在各種血流動力學條件下; [93] 它可以用於監測兒童 [94] 和機械輔助 [95] 患者。
Vigileo/FloTrac 系統 [Vigileo]
[edit | edit source]FloTrac/Vigileo (愛德華生命科學有限公司,美國) 是一種未校準的脈搏波分析系統,它使用專用壓力感測器 (FloTrac) 和監測器來計算心輸出量 (Vigileo)。它不需要獨立校準。心輸出量演算法基於心臟的弗蘭克-斯塔林定律,即主動脈脈壓 (PP) 與每搏輸出量 (SV) 成正比,與主動脈順應性成反比。該系統從任何標準外周動脈導管獲取壓力訊號。從動脈壓力中計算出 20 秒時間段內平均動脈壓 (MAP) 的標準差 (σAP)。此 σAP 與血管張力因子 (Khi) 相乘,以生成每搏輸出量。Khi 結合反映動脈阻力和順應性,順應性是一個多元多項式方程,它不斷量化動脈順應性和血管阻力。它透過分析患者的心率、標準差 σAP、平均動脈壓、壓力相關的動脈順應性以及使用 Langewouters 方程的患者人口統計資料來計算。簡化方程如下:
心輸出量透過將每搏輸出量乘以心率來計算。動脈壓力訊號處理的廣泛應用使得 FloTrac 演算法高度依賴於高保真壓力訊號。因此,透過測試以最佳化動脈導管的阻尼和沖洗來確保壓力監測訊號質量非常重要。
Modelflow 方法 [Modelflow]
[edit | edit source]Modelflow (FMS,阿姆斯特丹,荷蘭) 是一種三要素 Windkessel 模型,用於描述動脈迴圈:特徵阻抗代表主動脈對脈動流入的阻力,Windkessel 順應性代表主動脈對體積增加的阻力,外周阻力代表血管床對血液排出的阻力。更多細節可以在其他地方找到[97][98]。
超聲多普勒方法
[edit | edit source]經食道多普勒 [TOD]
[edit | edit source]
如今,經食道多普勒 (TOD) 是一種廣泛使用的超聲方法,用於手術期間的液體管理,有證據表明它可以改善患者預後[99][100][101][102][103][104][105][106],並已得到英國國家衛生與臨床卓越研究所 (NICE) 的推薦。 [107]
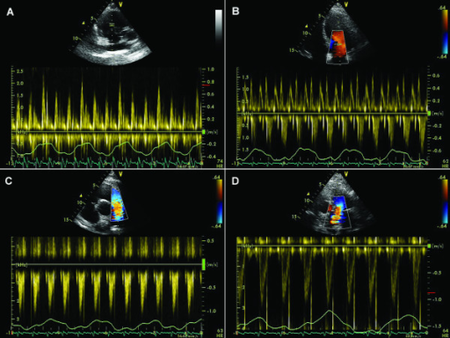
經食道多普勒探頭插入患者的食道,測量降主動脈中的血流速度。然後監測器顯示一個速度/時間波形,為臨床醫生提供資訊,以便在手術期間安全地管理患者的液體狀況。一個小的超聲換能器,安裝在柔性探頭的尖端,透過口腔或鼻腔放置在食道中,沿著降主動脈。根據插入路徑(口腔 vs 鼻腔),插入深度通常為成人 35 到 45 釐米。換能器透過旋轉指向主動脈,以獲得最佳主動脈速度訊號。血流速度透過多普勒方程計算。
其中 V 是血液速度,Fo 是發射頻率,Fd 是頻率變化(多普勒頻移),cosθ 是超聲波束方向與血流方向之間的夾角,c 是超聲波在血液中的速度。
一個侷限性是 ODM 測量的是血液速度而不是Q,並且依賴於根據患者年齡、身高和體重進行轉換的列線圖[108],將測量的速度轉換為每搏輸出量和心輸出量。
經胸多普勒 [TTE]
[edit | edit source]經胸多普勒 (TTD) 是一種完全非侵入性方法,它使用放置在頸靜脈切跡的超聲探頭來獲取左心室流出道的血流速度。該方法在原理上與經食道多普勒技術相同。心輸出量透過測量主動脈瓣的橫截面積以及流出道中的速度分佈來計算。然而,在一些受試者中可能很難識別主動脈根部。在這些情況下,可以使用肺動脈瓣的流出道。對準受操作員技術、解剖結構和受試者運動(例如,呼吸期間)的影響。
胸部電阻抗 [Bioimpedance]
[edit | edit source]電阻抗大約 50 年前被引入,作為一種廉價且非侵入性的心輸出量測量方法。透過兩個電極將低幅度的高頻交流電施加到胸部。使用放置在電流電極之間的另外兩個電極來測量產生的電壓。測量到的生物阻抗變化被認為與心臟相關的血容量變化有關。生物阻抗的變化可以轉換為心輸出量。
測量心輸出量的不同方法概述
[edit | edit source]表. 測量心輸出量的不同方法的特徵概述
| CO 方法 | 侵入性 | 響應 | 準確性 | 精確度 | 侷限性 |
|---|---|---|---|---|---|
| Fick O2 | +++ | 間歇 | 高 | 中等 | 需要 PAC 測量靜脈 O2 和肺活量計或機械呼吸機。勞動密集型技術 |
| Fick CO2 | + | 慢 | 低 | 低 | 受試者必須在呼吸機上,由於分流導致的誤差 |
| PAC Td 衝擊劑 | +++ | 間歇 | 高 | 高 | 機械通氣期間需要特殊預防措施,需要 PAC 和三次測量 |
| PAC CCO | +++ | 連續 | 中等 | 中等 | 需要 PAC 和三次測量 |
| TP Td 衝擊劑 | ++ | 間歇 | 高 | 高 | 需要 PAC 和三次測量 |
| TP Li 衝擊劑 | ++ | 間歇 | 中等 | 中等 | 只需要動脈導管,但需要三次測量才能與參考方法充分一致 |
| PiCCO | ++ | 逐搏 | 中等 | 中等 | 需要使用獨立(其他)方法進行頻繁校準 |
| LiDCO | ++ | 逐搏 | 中等 | 中等 | 需要使用獨立(其他)方法或鋰指示劑方法進行頻繁校準 |
| Vigileo | ++ | 逐搏 | 中等 | 高 | 需要專用感測器 |
| Modelflow | ++ | 逐搏 | 高 | 高 | 需要股動脈或橈動脈導管 |
| TOD | + | 逐搏 | 高 | 低 | 需要透過口腔或鼻腔進入食道 |
| TTE | - | 間歇 | 中等 | 低 | 操作員之間存在較大差異 |
| Bioimpedance | - | 間歇 | 低 | 低 | 由於解剖結構變化、分流、運動、電噪聲引起的偽影 |
來源:Bart F Geerts, Leon P Aarts, and Jos R Jansen. Methods in pharmacology: measurement of cardiac output,Br J Clin Pharmacol. Mar 2011; 71(3): 316–330.
血管電容描述了血管在跨壁壓力的變化下,其體積的變化情況。交感神經對靜脈的啟用會降低靜脈順應性,增加靜脈收縮張力,升高中心靜脈壓,並透過弗蘭克-斯達林機制間接促進靜脈迴流,該機制透過提高心輸出量,從而增加迴圈系統中的總血流量。在非常高的跨壁壓下,血管變得更加僵硬,跨壁壓力變化引起的體積變化量很小。由於所有血管都表現出這些非線性,因此沒有單個引數可以描述電容。因此,應考慮壓力-體積關係。

血管順應性 (C) 描述為壓力-體積關係的斜率。血管在跨壁壓力(內部壓力減去外部壓力)增加的情況下擴張並增加體積的能力被稱為血管順應性 (C),它被量化為體積變化 (ΔV) 除以壓力變化 (ΔP)。
在圖中,斜率不是線性的,因為血管壁是異質組織。這意味著順應性在更高的壓力和體積下降低。在較低的壓力下,靜脈的順應性大約是動脈的 10 到 20 倍。
容量定義為特定擴張壓力下血管中的血容量。它是無應力體積和應力體積的總和,。
當器官的流入和流出突然停止,血容量重新分配時,血管內所有壓力都相同。這種壓力稱為平均迴圈充盈壓 (Pmcf)。它受迴圈血量和靜脈系統壁平滑肌張力(決定系統容量)的影響。[109] 有時,動脈壓不等於靜脈壓,因為血流在測量操作期間必須從擴張的動脈血管移動到靜脈床,並且血流可能會在平衡之前停止。Pmcf 可以透過在動物中短暫誘發心臟驟停來實驗測量。實驗測量的平均迴圈充盈壓可以很好地估計 Pv(最小靜脈的壓力),用於估計靜脈應力體積。
血管阻力是指推動血液透過迴圈系統所必須克服的流動阻力。外周迴圈提供的阻力稱為全身血管阻力 (SVR)。肺血管提供的阻力稱為肺血管阻力 (PVR)。根據定義,它是靜脈迴圈入口(毛細血管)和靜脈流出之間的壓力梯度除以靜脈流速之比。
其中 R 是靜脈阻力,Pc 是毛細血管壓,Pra 是右心房壓,Q 是靜脈血流。
| 測量 | 參考範圍 | ||
|---|---|---|---|
| dyn·s/cm5 | MPa·s/m3 | mmHg·min/l 或 HRU/伍德單位 | |
| 全身血管阻力 | 700–1600[110] | 70–160[111] | 9–20[111] |
| 肺血管阻力 | 20–130[110] | 2–13[111] | 0.25–1.6[111] |
靜脈慣性 (I_v ) 是與加速或減速的血栓塊的質量相關的流量變化阻力。具有恆定橫截面積的圓柱形管的慣性 Iv 為 I_v= Lρ/A,其中 L 是血管長度,ρ 是血液密度,A 是橫截面積 [112]。
因此,全身血管阻力可以用 dyn·s·cm−5 單位計算為
其中平均動脈壓是舒張壓的 2/3 加上收縮壓的 1/3(或舒張壓 + 1/3(收縮壓-舒張壓))。
因此,肺血管阻力可以用 dyn·s·cm−5 單位計算為
其中,壓力以毫米汞柱 (mmHg) 為單位,心輸出量以升/分鐘 (L/min) 為單位。[113]
電容
[edit | edit source]順應性
[edit | edit source]
為了測量順應性,需要測量體積的變化。這比測量總血液量更容易。體積描記法可以用於測量人體不同部位的體積變化。它涉及使用血壓袖帶或其他感測器連線到稱為體積描記儀的機器上。
重量法
[edit | edit source]重量法非常簡單,並且對於測量血液體積變化非常有用。假設 1 克血液等於 1 毫升血液。如果器官可以被分離並用完整的血管稱重,就可以測量體積變化。
進一步閱讀
[edit | edit source]- Bronzino, Joseph D. (2006 年 4 月). 生物醫學工程手冊,第三版. [CRC 出版社]. ISBN 978-0-8493-2124-5.
- Villafane, Carlos, CBET. (2009 年 6 月). 生物醫學:從學生的角度看,第一版. [Techniciansfriend.com]. ISBN 978-1-61539-663-4.
{{cite book}}: CS1 maint: multiple names: authors list (link) - 與 生物醫學工程 相關的 資訊。
練習
[edit | edit source]參考文獻
[edit | edit source]- ↑ http://www.ivy-rose.co.uk/HumanBody/Blood/Heart_Structure.php
- ↑ 人體心臟解剖圖。檢索於 2010 年 7 月 2 日。
- ↑ http://www.americanheart.org/presenter.jhtml?identifier=4598
- ↑ a b >http://www.medicinenet.com/script/main/art.asp?articlekey=9122
- ↑ Szpak, Paul (2011). "魚骨化學和超微結構:對埋藏學和穩定同位素分析的影響". 考古科學雜誌. 38 (12): 3358–3372. doi:10.1016/j.jas.2011.07.022.
- ↑ Fratzl, P. (2008). 膠原蛋白:結構與力學. 紐約:施普林格。 ISBN 0-387-73905-X.
- ↑ Buehler, M. J. (2006). "自然設計堅韌的膠原蛋白:解釋膠原蛋白原纖維的奈米結構". PNAS. 103 (33): 12285–12290. Bibcode:2006PNAS..10312285B. doi:10.1073/pnas.0603216103. PMC 1567872. PMID 16895989.
- ↑ Junqueira's Basic Histology, P106
- ↑ https://en.wikipedia.org/wiki/Type_II_collagen
- ↑ https://en.wikipedia.org/w/index.php?title=Collagen,_type_III,_alpha_1&redirect=no
- ↑ Harper, J., Harper, E. 和 Covell, J.W.,微型豬體積負荷和壓力負荷誘導的心臟肥大中的膠原蛋白特徵,Am. J. Physiol., 265, H434–H438,1993。
- ↑ Iimoto, D.S., Covell, J.W. 和 Harper, E., 與體積負荷肥大相關的 I 型和 III 型膠原蛋白交聯增加,Circ. Res., 63, 399–408, 1988。
- ↑ Medugorac, I. 和 Jacob, R., 大鼠左心室膠原蛋白的特徵,Cardiovasc. Res., 17, 15–21, 1983
- ↑ Mukherjee, D. 和 Sen, S., 自發性高血壓大鼠心肌肥大發展和消退過程中的膠原蛋白表型,Circ. Res., 67, 1474–1480, 1990。
- ↑ Janeczko RA,Ramirez F(1989 年 10 月)。"人類 α1(III)膠原蛋白的完整核苷酸和氨基酸序列"。核酸研究。17(16):6742。doi:10.1093/nar/17.16.6742。PMC 318382。PMID 2780304.
- ↑ Superti-Furga A,Gugler E,Gitzelmann R,Steinmann B(1988 年 6 月)。"Ehlers-Danlos IV 型綜合徵:兩個 COL3A1 等位基因之一中的多外顯子缺失影響 III 型前膠原蛋白的結構、穩定性和加工"。J Biol Chem。263(13):6226–32。PMID 2834369.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ↑ Schlosser,Thomas;Pagonidis,Konstantin;Herborn,Christoph U.;Hunold,Peter;Waltering,Kai-Uwe;Lauenstein,Thomas C.;Barkhausen,Jörg(2005)。"使用 16-MDCT 和用於心內膜和心外膜邊界描繪的新軟體評估左心室引數"。Am J Roentgenol。184(3):765–773。doi:10.2214/ajr.184.3.01840765.
- ↑ Sosnovik DE,Wang R,Dai G,Reese TG,Wedeen VJ,心臟的擴散 MR 纖維束成像,J Cardiovasc Magn Reson(2009)
- ↑ Streeter DD,Spotnitz HM,Patel DP,Ross J,Sonnenblick EH。(1969)犬左心室舒張期和收縮期的纖維方向。Circ Res 24:339–347
- ↑ Streeter DD,Hanna WT。(1973)犬左心室心肌連續狀態的工程力學。II. 纖維角和肌節長度。Circ Res 33:656–664。
- ↑ Ross MA,Streeter DD。(1975)正常獼猴左心室非均勻的亞心內膜纖維方向。Eur J Cardiol 3:229–247
- ↑ Greenbaum RA,Yen Ho S,Gibson DG,Becker AE,Anderson RH。(1981)人的左心室纖維結構。Br Heart J 45:248–263。
- ↑ Arts T,Prinzen FW,Snoeckx LHEH,Rijcken JM,Reneman RS。(1994)細胞環境中機械反饋對心臟結構的適應:模型研究。Biophys J 66:953–961
- ↑ Arts T,Veenstra PC,Reneman RS。(1979)左心室力學模型。Ann Biomed Eng 7:299–318
- ↑ Bovendeerd PHM,Arts T,Huyghe JM,van Campen DH,Reneman RS。(1992)區域性左心室壁力學對心肌纖維方向的依賴性:模型研究。J Biomech 25:1129–1140。
- ↑ Chadwick RS。(1982)左心室力學。Biophys J 39:279–288
- ↑ Hsu,E.W.,Muzikant,A.L.,Matulevicius,S.A. 等人,直接組織學相關的磁共振心肌纖維方向圖譜,Am. J. Physiol.,274,H1627–H1634,1998
- ↑ Scollan,D.F.,Holmes,A.,Winslow,R. 等人,透過擴散張量磁共振成像獲得的心肌微結構的組織學驗證,Am. J. Physiol.,275,H2308–H2318,1998
- ↑ Dou,J.,Tseng,W.Y.,Reese,T.G. 等人,結合擴散和應變 MRI 揭示人體心肌層狀片層在體內的結構和功能,Magn. Reson. Med.,50,107–113,2003
- ↑ David E. Sosnovik,MD,Ruopeng Wang,MS,Guangping Dai,PhD,Teresa Wang,MS,Elena Aikawa,MD,PhD,Mikhael Novikov,MD,Anthony Rosenzweig,MD,Richard J. Gilbert,MD 和 Van J. Wedeen,MD,擴散譜 MRI 纖維束成像揭示梗塞心肌中存在複雜的殘餘肌纖維網路,迴圈:心血管成像。2009;2:206-212
- ↑ Barrett 等人。""Ganong's Review of Medical Physiology 24e""(2012)表 30-3
- ↑ Sagawa,K.,Maughan,L.,Suga,H. 等人,心臟收縮和壓力-容積關係。牛津大學出版社,1988
- ↑ Hill,A.V.(1938 年 10 月)。"肌肉的縮短熱和動力學常數"。Proc. R. Soc. Lond. B(倫敦:皇家學會)126(843):136–195。doi:10.1098/rspb.1938.0050
- ↑ Bers,D.M.,激-縮偶聯和心臟收縮力。克魯維爾
- ↑ Rüegg,J.C.,肌肉啟用中的鈣:比較方法,第 2 版。施普林格出版社,1988
- ↑ Tözeren,A.,肌肉收縮的連續介質流變學及其在心臟收縮力中的應用,Biophys. J.,47,303–309,1985
- ↑ a b Hunter,P.J.,McCulloch,A.D. 和 ter Keurs,H.E.,心臟肌肉的機械特性建模,Prog. Biophys. Mol. Biol.,69,289–331,1998
- ↑ Kentish,J.C.,Ter Keurs,H.E.D.J.,Ricciari,L. 等人,完整和剝離的大鼠右心室小梁的肌節長度-力關係之間的比較,Circ. Res.,58,755–768,1986
- ↑ "心臟瓣膜"。心臟和中風百科全書。美國心臟協會,Inc. 檢索於 2010-08-05.
{{cite web}}: 外部連結在|work= - ↑ Klabunde,RE(2009-07-02)。"壓力梯度"。心血管生理學概念。理查德·E·克拉布恩德. 檢索於 2010-08-06.
- ↑ Klabunde,RE(2007-04-05)。"心臟瓣膜病"。心血管生理學概念。理查德·E·克拉布恩德. 檢索於 2010-08-06.
- ↑ Christie,G.W. 1990. 主動脈心臟瓣膜小葉的解剖結構:戊二醛固定對功能的影響。Eur. J. Cardio-Thorac. Surg. 6[Supp 1]: S25–S33。
- ↑ Thubrikar,M. 1990. 主動脈瓣。CRC 出版社,佛羅里達州博卡拉頓。
- ↑ Westaby,S.,Karp,R.B.,Blackstone,E.H. 和 Bishop,S.P. 1984. 成人人類瓣膜尺寸及其手術意義。Am. J. Cardiol. 53: 552–556。
- ↑ Gramiak,R. 和 Shah,P.M. 1970. 正常和病變主動脈瓣的超聲心動圖。放射學 96: 1。
- ↑ Komoda,T.,Hetzer,R.,Uyama,C.,Siniawski,H.,Maeta,H.,Rosendahl,P. 和 Ozaki,K. 1994. 透過 3D 成像評估二尖瓣環功能,用於二尖瓣手術。J. Heart Valve Dis. 3: 483–490。
- ↑ Pai,R.G.,Tanimoto,M.,Jintapakorn,W.,Azevedo,J.,Pandian,N.G. 和 Shah,P.M. 1995. 使用經食道超聲心動圖技術的三維體繪製動態二尖瓣環解剖。J. Heart Valve Dis. 4: 623–627。
- ↑ Glasson,J.R.,Komeda,M.,Daughters,G.T.,Niczyporuk,M.A.,Bolger,A.F.,Ingels,N.B. 和 Miller,D.C. 1996. 左心室射血過程中正常二尖瓣環的三維區域動態。J. Thorac. Cardiovasc. Surg. 111: 574–585
- ↑ Silverman,M.E. 和 Hurst,J.W. 1968. 二尖瓣複合體:二尖瓣環、二尖瓣瓣葉、腱索和乳頭肌的解剖、生理和病理相互作用。Am.Heart J. 76: 399–418。
- ↑ Raganathan,N.,Lam,J.H.C.,Wigle,E.D. 和 Silver,M.D. 1970. 人體二尖瓣的形態:瓣葉。迴圈 41: 459–467
- ↑ Roberts,W.C. 1983. 正常和異常二尖瓣的形態學特徵。Am. J. Cardiol. 51:1005–1028
- ↑ Barlow,J.B. 1987. 二尖瓣的視角。F.A. Davis 公司,賓夕法尼亞州費城。
- ↑ Kunzelman,K.S.,Cochran,R.P.,Verner,E.D. 和 Eberhart,R.D. 1994. 二尖瓣建模的解剖學基礎。J. Heart Valve Dis. 3: 491–496。
- ↑ Kunzelman,K.S.,Cochran,R.P.,Murphee,S.S.,Ring,W.S.,Verrier,E.D. 和 Eberhart,R.C. 1993a. 二尖瓣中不同膠原蛋白的分佈及其對生物力學行為的影響。J. Heart Valve Dis. 2: 236–244
- ↑ Moore,K.L. 和 Agur,A.M. (2007). Essential Clinical Anatomy: Third Edition. 巴爾的摩:Lippincott Williams & Wilkins. 92. ISBN 978-0-7817-6274-8
- ↑ Moore,K.L. 和 Agur,A.M. (2007). Essential Clinical Anatomy: Third Edition. 巴爾的摩:Lippincott Williams & Wilkins. 94. ISBN 978-0-7817-6274-8
- ↑ a b 維基百科,血管.
- ↑ 富蘭克林研究所公司 "血液 - 人體心臟". 檢索於 2009 年 3 月 19 日.
- ↑ Gerard J. Tortora,Bryan Derrickson (2012). "心血管系統:血液"。Principles of Anatomy & Physiology, 13th。John Wiley & Sons, Inc. 第 729–732 頁。 ISBN 978-0470-56510-0.
{{cite book}}: 未知引數|ignore-isbn-error=被忽略 (|isbn=建議) (幫助)CS1 維護:使用作者引數 (連結) - ↑ Liepsch,D.,Thurston,G. 和 Lee,M. 1991. 模擬血液流變學特性的流體研究及其在動脈分支模型中的應用。生物流變學 28: 39
- ↑ Gerard J. Tortora,Bryan Derrickson (2012). "心血管系統:血管和血流動力學"。Principles of Anatomy & Physiology, 13th。John Wiley & Sons, Inc. 第 816 頁。 ISBN 978-0470-56510-0.
{{cite book}}: 未知引數|ignore-isbn-error=被忽略 (|isbn=建議) (幫助)CS1 維護:使用作者引數 (連結) - ↑ Wilkinson IB, Cockcroft JR, Webb DJ (1998). "脈搏波分析和動脈硬度". J. Cardiovasc. Pharmacol. 32 (Suppl 3): S33–7. PMID 9883745.
{{cite journal}}: CS1 維護:多個名稱:作者列表 (連結) - ↑ Nichols WW (2005 年 1 月). "從非侵入性壓力波形獲得的動脈硬度的臨床測量"。Am. J. Hypertens. 18 (1 Pt 2): 3S–10S. doi:10.1016/j.amjhyper.2004.10.009. PMID 15683725.
- ↑ Wilkinson IB, Fuchs SA, Jansen IM; 等人 (1998 年 12 月). "脈搏波速度和增強指數的重複性,透過脈搏波分析測量". J. Hypertens. 16 (12 Pt 2): 2079–84. doi:10.1097/00004872-199816121-00033. PMID 9886900.
{{cite journal}}: 明確使用等人:|author=(幫助)CS1 維護:多個名稱:作者列表 (連結) - ↑ Gosling, R.G.; Budge, M.M. (2003). "描述動脈彈性行為的術語"。Hypertension. 41 (6): 1180–1182. doi:10.1161/01.HYP.0000072271.36866.2A.
- ↑ Friedman,M.H.,Brinkman,A.M.,Qin,J.J. 等人。1993. 冠狀動脈幾何形狀與早期蘇丹嗜色性病變分佈之間的關係。動脈粥樣硬化 98:193。
- ↑ Klabunde, Richard E. "靜脈迴流 - 血流動力學". 心血管生理學概念. 檢索於 2011 年 3 月 8 日.
- ↑ Guyton, Arthur C.; John E. (John Edward) (2006). 醫學生理學教科書 (第 11 版). 費城:愛思唯爾公司. ISBN 0-7216-0240-1.
{{cite book}}: CS1 維護:作者列表有多個名稱 (連結)Template:Pn - ↑ Gorgeia 生理學,心輸出量的間接測量
- ↑ 維基百科,動脈血
- ↑ "動脈血氧差". 運動醫學、運動科學和運動機能學. 網路行業及其許可人. 2011. 檢索於 2011 年 4 月 30 日.
- ↑ Jansen JR. 熱稀釋法用於臨床評估心輸出量. 重症監護醫學. 1995;21:691–7.
- ↑ Breukers RB, Jansen JR. 肺動脈熱稀釋心輸出量與經肺熱稀釋心輸出量在兩名胸內病變患者中的比較. 斯堪的納維亞麻醉學報. 2004;48:658–61.
- ↑ Swan HJ, Ganz W, Forrester J, Marcus H, Diamond G, Chonette D. 使用流向導向氣囊尖導管進行人體心臟導管插入術. 新英格蘭醫學雜誌. 1970;283:447–51.
- ↑ a b Yelderman M. 使用隨機系統辨識技術連續測量心輸出量. 臨床監測雜誌. 1990;6:322–32.
- ↑ Aranda M, Mihm FG, Garrett S, Mihm MN, Pearl RG. 連續心輸出量導管:在控制流量變化後體外響應時間延遲. 麻醉學. 1998;89:1592–5.
- ↑ Tibby SM, Hatherill M, Marsh MJ, Morrison G, Anderson D, Murdoch IA. 使用股動脈熱稀釋法與直接費克法進行通氣兒童和嬰兒心輸出量測量臨床驗證. 重症監護醫學. 1997;23:987–91.
- ↑ Sakka SG, Bredle DL, Reinhart K, Meier-Hellmann A. 敗血症或敗血症休克患者血流動力學不穩定早期階段胸腔內血容量與心臟充盈壓的比較. 臨界護理雜誌. 1999;14:78–83.
- ↑ Pauli C, Fakler U, Genz T, Hennig M, Lorenz HP, Hess J. 兒童心輸出量測定:經肺熱稀釋法與直接費克原理的等效性. 重症監護醫學. 2002;28:947–52.
- ↑ Jansen JR, Schreuder JJ, Settels JJ, Kornet L, Penn OC, Mulder PG, Versprille A, Wesseling KH. 單次注射熱稀釋法. 流量校正方法. 麻醉學. 1996;85:481–90.
- ↑ Jansen JR, Schreuder JJ, Punt KD, van den Berg PC, Alfieri O. 熱稀釋法單次受控注射測定平均心輸出量. 重症監護醫學. 2001;29:1868–73.
- ↑ Band DM, Linton RA, O'Brien TK, Jonas MM, Linton NW. 人體心輸出量測量中所用指示劑稀釋曲線形狀. 生理學雜誌. 1997;498:225–9
- ↑ Jonas MM, Lint RAF, O'Brein TK, Band DM, Linton NW, Kelly F, Burden TJ, Chevalier SFA, Thompson RPH, Birch NJ, Powell JJ. 患者和正常志願者靜脈注射氯化鋰的藥代動力學. 痕量微探針技術雜誌. 2001;19:313–20.
- ↑ a b Cecconi M, Fawcett J, Grounds RM, Rhodes A. 一項前瞻性研究,評估脈搏動力分析在重症患者心輸出量監測中的準確性. BMC 麻醉學. 2008;8:3 無效的
<ref>標籤;名稱“CecconiM”定義多次,但內容不同 - ↑ Frank O. 動脈脈搏的基準形式第一篇論述:數學分析. 生物學雜誌. 1899:483–526
- ↑ Halvorsen PS, Sokolov A, Cvancarova M, Hol PK, Lundblad R, Tonnessen TI. 非體外迴圈冠狀動脈搭橋手術期間連續心輸出量:脈搏波形分析與肺動脈熱稀釋法的比較. 英國麻醉學雜誌. 2007;99:484–92.
- ↑ Johansson A, Chew M. 血流動力學不穩定期間連續脈搏波形心輸出量測量的可靠性. 臨床監測與計算雜誌. 2007;21:237–42.
- ↑ Hamzaoui O, Monnet X, Richard C, Osman D, Chemla D, Teboul JL. 在長達 6 小時的免校準期間內,血管張力變化對脈搏波形與經肺熱稀釋心輸出量測量一致性的影響. 重症監護醫學. 2008;36:434–40.
- ↑ de Wilde RB, Breukers RB, van den Berg PC, Jansen JR. 使用股動脈和橈動脈壓力波形監測心輸出量. 麻醉學. 2006;61:743–6.
- ↑ Jansen JR, Wesseling KH, Settels JJ, Schreuder JJ. 心臟手術期間脈搏波形連續心輸出量監測. 歐洲心臟雜誌. 1990;11(Suppl. I):26–32.
- ↑ Romano SM, Pistolesi M. 從人體全身動脈血壓評估心輸出量. 重症監護醫學. 2002;30:1834–41.
- ↑ Romano, Salvatore M.; Pistolesi, Massimo (2002). "從人體全身動脈血壓評估心輸出量". 重症監護醫學. 30 (8): 1834–41. doi:10.1097/00003246-200208000-00027. PMID 12163802.
- ↑ Scolletta, S.; Romano, S. M.; Biagioli, B; Capannini, G; Giomarelli, P (2005). "壓力記錄分析法 (PRAM) 用於測量各種血流動力學狀態下的心輸出量". 英國麻醉學雜誌. 95 (2): 159–65. doi:10.1093/bja/aei154. PMID 15894561.
- ↑ Calamandrei, Marco; Mirabile, Lorenzo; Muschetta, Stefania; Gensini, Gian Franco; De Simone, Luciano; Romano, Salvatore M. (2008). "兒童心輸出量評估:壓力記錄分析法與多普勒超聲心動圖的比較". 兒科重症監護醫學. 9 (3): 310–2. doi:10.1097/PCC.0b013e31816c7151. PMID 18446106.
- ↑ Scolletta, S.; Gregoric, I. D; Muzzi, L.; Radovancevic, B.; Frazier, O H. (2007). "脈搏波分析評估機械雙心室輔助期間的全身血流". Perfusion. 22 (1): 63–6. doi:10.1177/0267659106074784. PMID 17633137.
- ↑ Langewouters GJ, Wesseling KH, Goedhard WJ. 45 個體外人體胸主動脈和 20 個體外人體腹主動脈的靜態彈性特性及其新模型引數。J Biomech. 1984;17:425–35.
- ↑ Wesseling KH, Jansen JR, Settels JJ, Schreuder JJ. 利用非線性三元素模型計算人體主動脈壓力中的血流。J Appl Physiol. 1993;74:2566–73.
- ↑ Jansen JR, Schreuder JJ, Mulier JP, Smith NT, Settels JJ, Wesseling KH. 從主動脈壓力波推導的心臟輸出量與心臟手術患者的熱稀釋法的比較。Br J Anaesth. 2001;87:212–22.
- ↑ Mythen, Michael Gerard; Webb, A. R. (1995). "圍手術期血漿容量擴充減少心臟手術期間腸道粘膜灌注不足的發生率". Archives of Surgery. 130 (4): 423–9. doi:10.1001/archsurg.1995.01430040085019. PMID 7535996.
- ↑ Sinclair, Susan; James, Sally; Singer, Mervyn (1997). "術中血管內液體量最佳化和近端股骨骨折修復後住院時間:隨機對照試驗". BMJ. 315 (7113): 909–12. doi:10.1136/bmj.315.7113.909. PMID 9361539.
- ↑ Conway, D. H.; Mayall, R.; Abdul-Latif, M. S.; Gilligan, S.; Tackaberry, C. (2002). "隨機對照試驗調查在腸道手術期間使用食管多普勒監測的靜脈輸液滴定對結果的影響". Anaesthesia. 57 (9): 845–9. doi:10.1046/j.1365-2044.2002.02708.x. PMID 12190747.
- ↑ Gan, Tong J.; Soppitt, Andrew; Maroof, Mohamed; El-Moalem, Habib; Robertson, Kerri M.; Moretti, Eugene; Dwane, Peter; Glass, Peter S. A. (2002 年 10 月). "目標導向的術中液體管理減少了重大手術後的住院時間". Anesthesiology. 97 (4): 820–6. PMID 12357146.
- ↑ Venn, R.; Steele, A; Richardson, P; Poloniecki, J; Grounds, M; Newman, P (2002). "隨機對照試驗調查液體挑戰對髖部骨折患者住院時間和圍手術期發病率的影響". British Journal of Anaesthesia. 88 (1): 65–71. doi:10.1093/bja/88.1.65. PMID 11881887.
- ↑ Wakeling, H. G.; McFall, M. R.; Jenkins, C. S.; Woods, W. G.; Miles, W. F.; Barclay, G. R.; Fleming, S. C. (2005). "術中食管多普勒引導的液體管理縮短了重大腸道手術後的術後住院時間". British Journal of Anaesthesia. 95 (5): 634–42. doi:10.1093/bja/aei223. PMID 16155038.
- ↑ Noblett, S. E.; Snowden, C. P.; Shenton, B. K.; Horgan, A. F. (2006). "隨機臨床試驗評估多普勒最佳化液體管理對選擇性直腸切除術後結果的影響". British Journal of Surgery. 93 (9): 1069–76. doi:10.1002/bjs.5454. PMID 16888706.
- ↑ Pillai, Praveen; McEleavy, Irene; Gaughan, Matthew; Snowden, Christopher; Nesbitt, Ian; Durkan, Garrett; Johnson, Mark; Cosgrove, Joseph; Thorpe, Andrew (2011). “經多普勒最佳化的手術中液體管理對根治性膀胱切除術後結局影響的雙盲隨機對照臨床試驗”. 泌尿外科雜誌. 186 (6): 2201–6. doi:10.1016/j.juro.2011.07.093. PMID 22014804.
- ↑ http://www.nice.org.uk/mtg3Template:Full
- ↑ Lowe, Graham D.; Chamberlain, Barry M.; Philpot, Eleanor J.; Willshire, Richard J. (2010). “食道多普勒監測(ODM)引導的個體化目標導向液體管理(iGDFM)在手術中的應用——技術綜述” (PDF). Deltex Medical 技術綜述.
- ↑ Rothe, CF (1993年2月). “平均迴圈充盈壓:其意義和測量”. 應用生理學雜誌. 74 (2): 499–509. PMID 8458763.
{{cite journal}}: Cite has empty unknown parameters:|laydate=,|laysummary=, and|laysource=(help) - ↑ a b 表 30-1 in: Trudie A Goers; 華盛頓大學醫學院外科系; Klingensmith, Mary E; Li Ern Chen; Sean C Glasgow (2008). 華盛頓外科手冊. 費城:沃爾特斯·克魯維爾健康/利平科特·威廉姆斯與威爾金斯. ISBN 0-7817-7447-0.
{{cite book}}: CS1 maint: multiple names: authors list (link) - ↑ a b c d 源自 dyn·s/cm5 中的值
- ↑ Rose, W. 和 Shoukas, A.A. 1993. 體系靜脈和動脈阻抗的雙埠分析。 美國生理學雜誌. 265 (心血管生理學 34): H1577
- ↑ 維基百科,血管阻力





![{\displaystyle [C_{50}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e4ebfc9e24207df406d65e938a2fca3a52e24465)

![{\displaystyle {\frac {T_{0}}{T_{max}}}={\frac {[Ca]^{n}}{[Ca]^{n}+C_{50}^{n}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1a88c2eff0b1d57af482ccf7900fd686fcdbe789)
![{\displaystyle n=4.25[1+1.95(L/L_{ref}-1)]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ac20fe595473c6e175d80d6f26f9fb4a1fedbfde)
![{\displaystyle pC_{50}=-\log _{10}C_{50}=5.33[1+0.31(L/L_{ref}-1)]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a535e68abf10d2339778ea10306dd829de9630d2)