有機化學/胺

胺是有機化合物,含有並通常以一個或多個氮原子為基礎。從結構上看,胺類似於氨,氮可以鍵合多達三個氫原子,但胺還具有基於其碳連線的其他性質。在胺中,氨的一個或多個氫原子被有機取代基(如烷基(烷烴鏈)和芳基(芳香環)基團)取代。
另一種型別有機分子含有氮,但嚴格來說不是胺:含有一個三價(三鍵)氨基的羧酸衍生物實際上是醯胺而不是胺。醯胺和胺具有不同的結構和性質,因此這種區別實際上非常重要。含有金屬的有機氮化合物也稱為醯胺,因此,如果你看到一個分子中有一個氮原子,並且在該氮原子的旁邊有一個羰基或金屬,那麼你知道該分子應該是醯胺而不是胺。
以下實驗室方法可被認為是胺化合物製備的常用方法
- 醛肟或酮肟用鈉和乙醇還原得到相應的伯胺
H
|
R-C=N - OH + H ----> Na / Ethanol R-CH2-NH2 + H2O

- 透過 Staudinger 還原生成疊氮化物。
- 烯丙基胺可以由胺在 Aza-Baylis-Hillman 反應中製備。
用於製備伯胺。芳香伯胺不能用這種方法制備,因為芳基滷代物不與鄰苯二甲醯亞胺鉀發生親核取代反應。
該反應僅適用於伯胺的製備,它能提供不含其他胺的高產率伯胺。
- R3N+CH2CH2R' + OH- → R3N + H2C=CHR' + H2O
- 季銨鹽在強鹼的作用下會發生霍夫曼消除反應。
- 腈在鎳催化劑存在下用氫還原成胺,儘管應避免酸性或鹼性條件,以防止-CN基團可能的水解。
- LiAlH4更常用於實驗室規模的腈還原。
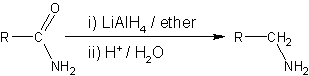
- 類似地,LiAlH4將醯胺還原為胺。
伯胺也可以透過氨的烷基化合成。滷代烷與胺反應生成相應的烷基取代胺,並釋放鹵化氫。這種反應對烷基碘化物和溴化物最為有用,但很少使用,因為烷基化的程度很難控制。如果反應胺是叔胺,則會生成季銨陽離子。許多季銨鹽可以透過這條途徑以不同的R基團和許多鹵化物和擬鹵化物陰離子來製備。

胺可以是伯胺、仲胺或叔胺,這取決於連線到它們上的含碳基團的數量。如果只有一個含碳基團(例如在分子CH3NH2中),則該胺被認為是伯胺。兩個含碳基團使胺成為仲胺,三個基團使它成為叔胺。利用氮的孤對電子,有時在能量上有利於使用氮作為親核試劑,從而將第四個含碳基團繫結到胺上。在這種情況下,它可以被稱為季銨離子。
伯胺
|
仲胺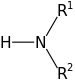
|
叔胺
|
具有多個胺基的有機化合物根據所連線的胺基(也稱為氨基)數量稱為二胺、三胺、四胺等等。例如,亞甲基二胺(也稱為二氨基甲烷)的化學式如下:H2N-CH2-NH2
芳香胺具有直接連線到芳香環結構的氮原子。由於其吸電子性質,芳香環極大地降低了胺的鹼性 - 並且這種效應可以根據環和氮上的取代基來增強或抵消。氮的孤對電子的存在對芳香環本身有相反的效果;因為氮原子可以將電子密度“借給”環,因此環本身對其他型別的化學反應變得更加活潑。
對於伯胺,如果胺不是主要特徵基團,則使用字首“氨基-” 。例如:4-氨基苯甲酸,其中羧酸是主要特徵基團。否則,使用字尾“-胺”,並使用母體雜化物或R基團取代基名稱。例如:乙胺或乙胺。或者,可以將字尾“-氮烷”附加到R基團取代基名稱:例如:丙氮烷。
對於仲胺、叔胺和季銨鹽,命名規則略有不同,但字尾相同。對於對稱胺,根據取代基是2個還是3個,使用“二”或“三”字首。例如,二丙胺是仲胺,三苯胺是叔胺。對於不對稱胺,母鏈得到“-胺”字尾。然後,此名稱以“N-”(表示氮鍵)和每個取代基的取代基組名稱為字首,對於叔醯胺,使用字母順序。例如,N-乙基-N-甲基-丙胺,而不是N-甲基-N-乙基-丙胺。
總結
- 作為字首:“氨基-”
- 作為字尾:“-胺”
- 字首“N-”表示在氮原子上進行取代(在仲胺、叔胺和季銨鹽的情況下)
一些常見胺的系統名稱
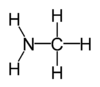 甲胺 |
正如人們很容易猜到的那樣,在原本只包含碳和氫原子的分子中加入氮等雜原子,會對胺的性質產生相當大的影響,與烷烴相比。
氫鍵對伯胺和仲胺以及所有胺的質子化衍生物的性質有很大影響。因此,胺的沸點高於相應的膦(含有磷的化合物),但通常低於相應的醇。醇或烷醇類似於胺,但具有 -OH 基團代替 NR2。由於氧的電負性比氮強,因此 RO-H 通常比相關的 R2N-H 化合物更酸性。
甲胺、二甲胺、三甲胺和乙胺在標準條件下為氣體。大多數常見的烷基胺是液體,而高分子量胺在標準溫度下自然是固體。此外,氣態胺具有特徵性的氨氣味,而液態胺具有獨特的“魚腥味”。
大多數脂肪胺在水中具有一定的溶解性,反映了它們形成氫鍵的能力。溶解度隨著分子中碳原子數量的增加而相對成比例地降低,尤其是在碳原子數量大於六個時。脂肪胺也表現出在有機溶劑中的顯著溶解性,特別是在極性有機溶劑中。然而,伯胺會與酮類化合物(如丙酮)發生反應,並且大多數胺與氯仿和四氯化碳作為溶劑溶液不相容。
芳香胺的孤對電子與苯環發生共軛(“共享”),因此它們參與氫鍵形成的趨勢有所減弱。由於這些分子的尺寸通常較大,因此它們的沸點通常比其他較小的胺略高。它們在水中的溶解度也往往相對較低,儘管它們保留在其他有機溶劑中的溶解性。
芳香共軛胺通常具有相當大的毒性,並且有可能透過皮膚輕鬆吸收,因此應始終將其視為“危險品”。

NHRR' 和 NRR'R" 型叔胺不是手性的:儘管氮原子帶有四個不同的取代基,包括孤對電子,但孤對電子可以“翻轉”穿過氮原子並反轉其他分子。這種帶有孤對電子的立體中心的瓦爾登翻轉的能量勢壘相對較低,例如三烷基胺約為 ~7 kcal/mol,因此很難使用叔胺獲得可靠的手性產物。由於這種低勢壘,NHRR' 等胺不能被光學拆分,而 NRR'R" 只有當 R、R' 和 R" 基團在環狀結構中受到限制時才能被光學拆分。季銨結構,例如 H3C-N+-RR'R",是手性的,並且可以很容易地被光學拆分。
與氨類似,胺作為鹼,並且相當強(參見提供的表格中一些共軛酸 Ka 值的示例)。胺的鹼性因分子而異,主要取決於
- 氮原子孤對電子的可用性
- 連線的取代基的電子性質(例如,烷基增強鹼性,芳基減弱鹼性等)
- 質子化胺的溶劑化程度,主要取決於反應中使用的溶劑
典型胺的氮原子具有一個孤對電子,它可以與氫離子 (H+) 結合以形成銨離子 -- R3NH+。簡單胺的水溶性很大程度上是由於水分子上的質子和這些孤對電子之間可能發生的氫鍵形成能力。
---
- 烷基的誘導效應
| 化合物的離子 | Kb |
|---|---|
| 氨 NH3 | 1.8·10-5 M |
| 甲胺 CH3NH2 | 4.4·10-4 M |
| 丙胺 CH3CH2CH2NH2 | 4.7·10-4 M |
| 異丙胺 (CH3)2CHNH2 | 5.3·10-4 M |
| 二乙胺 (CH3)2NH2 | 9.6·10-4 M |
烷基的 +I 效應提高了孤對電子的能量,從而提高了鹼性。
- 共軛效應 芳香體系
| 化合物的離子 | Kb |
|---|---|
| 氨 NH3 | 1.8·10-5 M |
| 苯胺 C6H5NH2 | 3.8·10-10 M |
| 4-甲基苯胺 4-CH3C6H4NH2 | 1.2·10-9 M |
芳香環的 +M 效應將孤對電子離域到環中,導致鹼性降低。
質子化胺的質子化程度
| 化合物的離子 | 氫鍵的最大數量 |
|---|---|
| NH4+ | 4 在 H2O 中非常可溶 |
| RNH3+ | 3 |
| R2NH2+ | 2 |
| R3NH+ | 1 在 H2O 中溶解度最低 |
醯氯和酸酐在沒有加熱的情況下與伯胺和仲胺反應生成醯胺。叔胺由於沒有可替換的氫原子而不能醯化。對於活性較低的苯甲醯氯,仍可以透過使用過量的鹼性水溶液來促進反應,進行醯化。
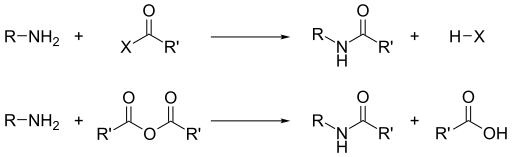
由於胺是鹼性的,它們會中和羧酸形成相應的銨羧酸鹽。在 200°C 加熱時,伯胺和仲胺鹽會脫水生成相應的醯胺。
胺 R3N 與強酸(如氫碘酸 (HI)、氫溴酸 (HBr) 和鹽酸 (HCl))反應生成銨鹽 R3NH+。
亞硝酸的化學式為 HNO2,不穩定。通常,它是在 NaNO2 和強酸(如 HCl 或 H2SO4)的稀溶液中間接產生的,以便 H+ 離子與溶液中的 NO2- 離子結合。
伯脂肪胺與亞硝酸反應生成非常不穩定的重氮鹽,重氮鹽會自發分解,失去 N2 生成碳正離子。碳正離子繼續生成烯烴、醇或滷代烷的混合物,其中醇是主要產物。這種反應在合成上幾乎沒有意義,因為即使在相當冷的條件下,形成的重氮鹽也太不穩定了。
- NaNO2 + HCl → HNO2 + NaCl

- 伯芳香胺,如苯胺(苯胺)在 0–5°C 形成更穩定的重氮離子。高於 5°C,它會分解生成苯酚和 N2。重氮鹽可以以結晶形式分離,但通常在溶液中使用,並在製備後立即使用,因為即使在微弱的周圍環境熱量下,重氮鹽也會在放置時迅速分解。固體重氮鹽在受到撞擊或輕微加熱時可能具有爆炸性。

- 伯胺與羰基化合物反應生成亞胺。具體來說,醛變成醛亞胺,酮變成酮亞胺。在甲醛 (R' = H) 的情況下,亞胺產物通常是環狀三聚體。
- RNH2 + R'2C=O → R'2C=NR + H2O
- 仲胺與酮和醛反應生成烯胺。烯胺包含一個 C=C 雙鍵,其中第二個 C 單鍵連線到 N,作為胺配體的一部分。
- R2NH + R'(R"CH2)C=O → R"CH=C(NR2)R' + H2O
伯芳香胺用作生產偶氮染料的起始原料。它們與亞硝酸反應生成重氮鹽,重氮鹽可以進行偶聯反應生成偶氮化合物。由於偶氮化合物顏色鮮豔,因此廣泛用於染色工業。例如:
- 甲基橙
- 直接棕 138
- 日落黃 FCF
- 胭脂紅
- 氯苯那敏 是一種抗組胺藥,有助於緩解因感冒、花粉症、皮膚瘙癢、昆蟲叮咬和蜇傷引起的過敏性疾病。
- 苯海拉明 是常見的抗組胺藥,即苯海拉明。
- 氯丙嗪 是一種鎮靜劑,可以鎮靜而不引起睡眠。它用於緩解焦慮、興奮、煩躁不安,甚至精神障礙。
- 對乙醯氨基酚 也稱為撲熱息痛或對乙醯氨基酚,是一種止痛藥,可以緩解頭痛等疼痛。據信它對胃的腐蝕性較低,是阿司匹林的替代品。
- IUPAC 命名法 用於胺的官方命名規則。

