有機化學/酮和醛
醛 (![]() ) 和酮 (
) 和酮 (![]() ) 都是羰基化合物。它們是有機化合物,其中羰基碳連線到羰基碳由 H 原子滿足,而酮則由碳滿足其兩個空位。
) 都是羰基化合物。它們是有機化合物,其中羰基碳連線到羰基碳由 H 原子滿足,而酮則由碳滿足其兩個空位。
酮的命名是將烷烴名稱中的-e替換為-one。碳鏈的編號使得酮碳,稱為羰基,獲得最小的數字。例如,![]() 將被命名為 2-丁酮,因為其根結構是丁烷,並且酮基位於第二碳上。
將被命名為 2-丁酮,因為其根結構是丁烷,並且酮基位於第二碳上。
或者,酮的官能團命名法也被 IUPAC 認可,其方法是按字母順序命名連線到羰基的取代基,最後加上“酮”字。上述 2-丁酮的例子也可以用這種方法命名為乙基甲基酮。
如果同一個結構上存在兩個酮基,則將在烷烴名稱後面新增-dione,例如庚烷-2,5-二酮。
醛將烷烴的-e結尾替換為-al表示醛。由於醛總是位於編號為一的碳上,因此不需要數字表示。例如,戊烷的醛將簡稱為戊醛。
醛的 -CH=O 基團被稱為甲醯基。當甲醯基連線到環上時,環的名稱後面加上字尾“甲醛”。例如,帶有甲醯基的己烷環被稱為環己烷甲醛。
醛和酮的極性以其羰基的高偶極矩為特徵,這使得它們成為相當極性的分子。它們比烯烴和醚更極性,儘管由於它們缺乏氫,它們不能像醇那樣參與氫鍵,因此它們的相對沸點高於烯烴和醚,但低於醇。
羰基與其取代基之間的典型鍵角顯示出與 120 度的三面角輕微偏差,其中 O=C-R 鍵之間的鍵角略高於羰基碳上的 R-C-R 鍵(其中 R 為任何取代基)。
該反應使用吡啶鎓氯鉻酸 (PCC) 在無水條件下進行(如果有水存在,醇將進一步氧化為羧酸)。
斯蒂芬還原
[edit | edit source]
這裡使用硫作為毒化劑,以防止生成的醛氧化成羧酸。更多詳細資訊請參見維基百科文章。
羅森蒙德反應
[edit | edit source]
(使用二甲苯作為溶劑)
製備酮
[edit | edit source]從格氏試劑
[edit | edit source]
R' R' OH
| | |
| | | O-R' OR' OR'
從腈
[edit | edit source]RCN + R'MgX ----> RCOR'(水解後) HCN 不與 RMgX 反應,因為 HCN 具有酸性氫,導致形成 RH。
從偕二鹵代烴
[edit | edit source]RCCl2R + 強鹼 ----> RCOR
奧彭瑙氧化
[edit | edit source]試劑是叔丁醇鋁,溶劑是丙酮
ROH + 丙酮 ----> 酮 + 異丙醇這種氧化不會影響雙鍵,在這種氧化中酮起氧化劑的作用,這與梅爾溫-龐多夫還原正好相反
芳香族化合物的傅-克醯基化
[edit | edit source]芳香環在 AlCl3 的存在下與羧酸氯 (RCOCl) 反應,形成 ArCOR 形式的芳基酮。
仲醇氧化成酮
[edit | edit source]仲醇可以使用酸化的重鉻酸鉀 (VI) 氧化成酮,並在迴流下加熱。
橙色的重鉻酸根離子 (VI),Cr2O72-,被還原成綠色的 Cr3+(aq) 離子。
烯烴的臭氧化反應
[edit | edit source]臭氧化反應是指雙鍵完全斷裂,烯烴分子轉化為兩個較小的分子。

臭氧化反應(臭氧裂解)分兩個步驟進行:首先,臭氧加成到雙鍵上,形成臭氧化物;其次,臭氧化物水解生成裂解產物。
將臭氧氣體通入四氯化碳等惰性溶劑中的烯烴溶液中;蒸發溶劑,將臭氧化物留下,形成粘稠的油狀物。這種不穩定、易爆的化合物不能提純,但可以直接用水分解,通常在還原劑存在下進行。如果使用氧化劑,可氧化醛或酮,如果可氧化,可進一步氧化成羧酸,而還原劑則不會這樣
在裂解產物中,每個原來雙鍵的碳原子都連線著一個雙鍵的氧原子。
還原劑的作用是防止過氧化氫的形成,過氧化氫會與醛和酮反應。(醛類,RCHO,通常為了便於分離而轉化為酸,rCOOH。)
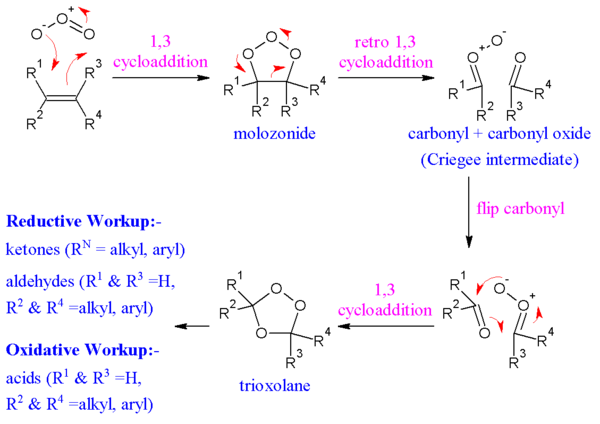
烯烴和臭氧透過 1,3-偶極環加成反應形成中間產物臭氧化物。接下來,臭氧化物透過逆向 1,3-偶極環加成反應轉化為相應的羰基氧化物(也稱為克里格中間體或克里格兩性離子)和醛或酮。氧化物與醛或酮再次透過 1,3-偶極環加成反應或生成相對穩定的臭氧化物中間體(三氧雜環戊烷)。
在強酸中,水被加到炔烴中。所用的強酸是硫酸和汞酸。
在酸 (H+) 或鹼 (OH-) 的存在下,醛或酮會與烯醇形成平衡,其中羰基的雙鍵遷移形成羰基和 α (α) 碳之間的雙鍵。
在酸的存在下,氧基團會發生質子化,水會奪取 α (α) 氫。
在鹼的存在下,α 氫會發生去質子化,水中的氫會被羰基氧奪取。
這是酮和醛的一個重要特徵,被稱為酮-烯醇互變異構或酮-烯醇互變異構,即羰基化合物在兩種形式之間的平衡。
必須強調的是,酮和烯醇形式是兩種不同的化合物,而不是異構體。它們被稱為彼此的互變異構體。這種平衡的存在需要 α-氫:那些不擁有 α-氫的化合物被稱為不可烯醇化酮。

由於醛和酮含有極性羰基,部分帶正電的碳原子可以充當親電試劑。強親核試劑和弱親核試劑都能進攻這個羰基碳,從而導致分子發生淨加成反應。
與氰化物反應,發生親核加成反應生成羥基腈
RR'C=O + CN- + H+ → RR'COHCN
例如丙酮 → 2-羥甲基丙腈
部分帶負電的氧原子可以充當親核試劑,或被親電試劑進攻。
使用強氧化劑,例如託倫試劑 (Ag2O 在氨水中) 酸化的重鉻酸鹽,貝內迪克特/菲林試劑 (本質上是鹼性的 Cu+2);醛類可以被氧化成羧酸,而酮類不能。這是一種測試樣品化合物中是否存在醛的方法:醛類與託倫試劑反應後會變成羧酸,而酮類則不會反應。當醛類與菲林試劑反應時,會得到紅色沉澱(由於形成了 Cu2O)。
羰基具有很強的吸電子性,相鄰的碳原子受誘導的影響。以羰基為參考,相鄰的碳原子使用希臘字母命名,按照與羰基的距離順序。α (α) 碳直接連線到羰基,β (β) 碳連線到 α 碳,γ (γ) 連線到 β (β),以此類推。
由於部分正電荷的誘導效應,特別容易被去除。

![{\displaystyle {\ce {Ca(COOH)2 ->[\Delta] HCHO + CaCO3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/983fac4505bd08deb768212f69be798055511c3c)
![{\displaystyle {\ce {(CH3COO)2Ca ->[\Delta] CH3COCH3 + CaCO3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/bee224b17e51525120e9299f41f75d79973725df)

![{\displaystyle {\ce {R-CN + SnCl2 + HCl -> R-CH=NH2+Cl- ->[H^+/H_2O] R-CHO}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f918cc742d9d4334dd7133ca4ccf2bbb84ded049)


