有機化學/光譜學
有幾種光譜技術可用於識別有機分子:紅外 (IR)、質譜 (MS) 紫外可見光譜 (UV/Vis) 和核磁共振 (NMR)。
IR、NMR 和 UV/vis 光譜基於觀察分子吸收和發射的電磁輻射的頻率。MS 基於測量分子的質量以及在 MS 儀器中可能產生的任何分子碎片的質量。
紫外可見光譜是一種吸收光譜技術,它利用 10 奈米到 700 奈米範圍內的電磁輻射。這些波長之間光的能量可以被駐留在分子軌道中的非鍵合 n 電子和 π 電子吸收。這種能量的吸收會導致電子從最高佔據分子軌道 (HOMO) 躍遷到最低未佔據分子軌道 (LUMO)。更具體地說,據說電子經歷了 n→π* 躍遷或 π→π* 躍遷。正是這種可見光能量的吸收導致了色素化合物的感知顏色。由於這種現象,UV/Vis 是一種經常在有機化學中使用的技術,用於識別分子中是否存在自由電子或雙鍵 (π) 鍵。分子最吸收的波長被稱為 λ-max,正是這個數字可以用來對不同分子進行比較分析。這種光譜技術也可以使用 Woodward-Fieser 規則來識別一些具有大的共軛 π 系統或羰基的分子,該規則依賴於一組經驗值來預測化合物的 λ-max。
核磁共振 (NMR) 波譜是確定有機化合物結構最有用的一種分析技術。NMR 主要有兩種型別:1H-NMR(質子 NMR)和13C-NMR(碳 NMR)。NMR 基於原子核具有稱為自旋的量子性質這一事實。當對 1H 或 13C 核施加磁場時,核可以與施加的磁場平行 (自旋 +1/2) 或反平行 (自旋 -1/2) 排列。
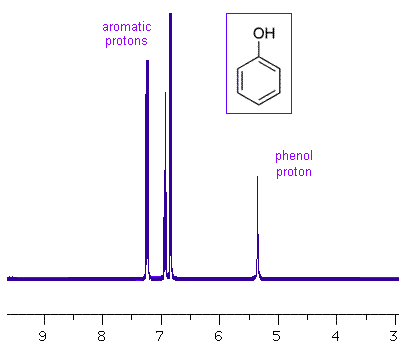
這兩個狀態具有不同的勢能,能量差取決於磁場強度。然而,原子核周圍磁場的強度取決於原子核周圍的化學環境。例如,原子核周圍和附近的負電荷電子可以遮蔽原子核免受磁場的影響,從而降低原子核感受到的有效磁場強度。這反過來將降低在 +1/2 和 -1/2 狀態之間躍遷所需的能量。因此,連線到供電子基團(如烷基)的原子核的躍遷能量將更低,而連線到吸電子基團(如羥基)的原子核的躍遷能量將更高。
在 NMR 機器中,被分析的化合物被放置在一個強磁場中,並用無線電波照射,使所有 1H 和 13C 原子核都佔據高能的 -1/2 狀態。當原子核恢復到 +1/2 狀態時,它們會釋放出與兩種自旋狀態之間的能量差相對應的無線電波。無線電波被記錄下來,並由計算機分析以給出樣品的強度與頻率圖。然後,可以使用這些資訊來確定化合物的結構。
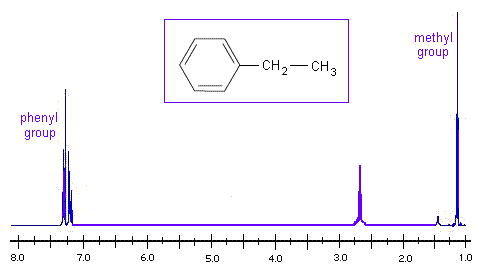
H-NMR 中的芳香族 供電子基團與吸電子基團
在單取代環上,供電子基團在較高的化學位移處共振。供電子基團透過將電子釋放到反應中心來增加電子密度,從而穩定碳正離子。甲基 (-CH3) 是供電子基團的一個例子。
相應地,吸電子基團在較低的化學位移處表示。吸電子基團將電子從反應中心拉走。這可以穩定富電子碳負離子。鹵素 (-Cl, -F) 和羧酸 (-COOH) 是吸電子基團的一些例子。
觀察乙苯的 H NMR 譜,我們可以看到甲基是最強的吸電子基團,因此它出現在最低的化學位移處。芳香苯基是最強的供電子基團,因此它具有最高的化學位移。
二取代環
整個芳香區域的積分強度值的總和顯示了有多少取代基連線到環上,因此總值為 4 表明環具有 2 個取代基。當苯環具有兩個取代基時,每個取代基都會對隨後的取代反應產生影響。引入新取代基的位點取決於現有基團的取向及其各自的導向效應。對於二取代苯環,有三種可能的 NMR 模式。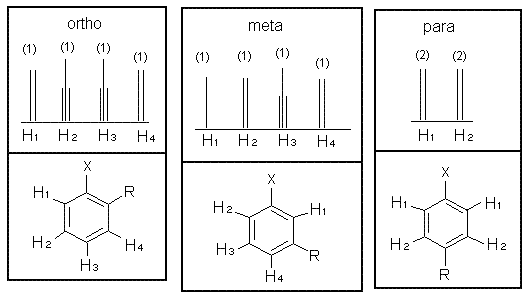
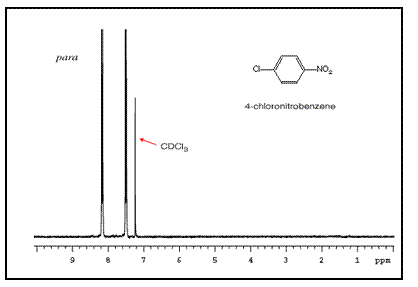
請注意,對位取代環通常顯示兩組對稱的峰,看起來像雙峰。
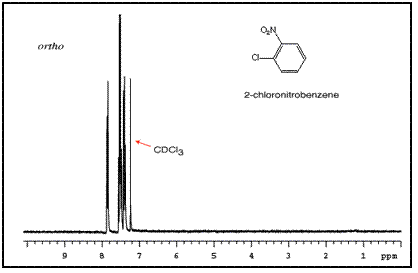
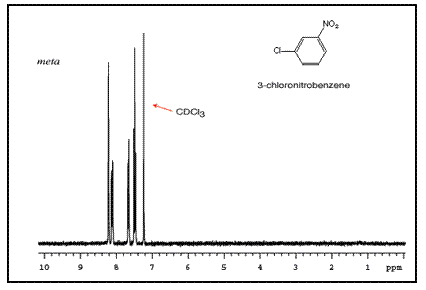
這些峰的順序取決於兩個取代基的性質。例如,氯硝基苯異構體的三個 NMR 譜如下
質譜儀測量離子相對於電荷的精確質量。很多時候,會事先進行某種形式的分離,從而能夠在相對純淨的樣品上收集光譜。可以將有機樣品引入質譜儀並使其電離。這也將一些分子分解成更小的碎片。
所得的質譜顯示
1) 最重的離子只是電離的分子本身。我們可以簡單地記錄它的質量。
2) 其他離子是分子的碎片,並提供有關其結構的資訊。常見的碎片是
| 種類 | 公式 | 質量 |
| 甲基 | CH3+ | 15 |
| 乙基 | C2H5+ | 29 |
| 苯基 | C6H5+ | 77 |
吸收紅外輻射使共價鍵振動。不同型別的鍵吸收不同波長的紅外線
紅外光譜學家不是記錄波長,而是記錄波數;在一釐米中能容納的波數。(這很容易轉換為波的能量。)
出於某種原因,光譜是反向記錄的(從 4000 到 500 cm-1 是典型的),通常在 1000 cm-1 以下使用不同的刻度(以便更清楚地看到指紋區域),並且顛倒(記錄的是 % 輻射透射率而不是輻射吸收率)。
吸收的 IR 輻射的波數是許多鍵的特徵,因此 IR 光譜可以確定樣品中包含哪些官能團。例如,羰基 (C=O) 鍵將在 1650-1760cm-1 處吸收。
| 鍵 | 最小波數 (cm-1) | 最大波數 (cm-1) | 官能團(以及其他注意事項) |
| C-O | 1000 | 1300 | 醇和酯 |
| N-H | 1580 | 1650 | 胺或醯胺 |
| C=C | 1610 | 1680 | 烯烴 |
| C=O | 1650 | 1760 | 醛、酮、酸、酯、醯胺 |
| O-H | 2500 | 3300 | 羧酸(非常寬的帶) |
| C-H | 2850 | 3000 | 烷烴 |
| C-H | 3050 | 3150 | 烯烴(將強度與烷烴進行比較,以大致瞭解所涉及的 H 原子的相對數量。) |
| O-H | 3230 | 3550 | 醇中的氫鍵 |
| N-H | 3300 | 3500 | 胺或醯胺 |
| O-H | 3580 | 3670 | 醇中的遊離 –OH(僅在用非極性溶劑稀釋的樣品中) |
列出的吸收以 cm-1 為單位。


產生一束紅外光,並將其分成兩束獨立的光束。一束穿過樣品,另一束穿過參考,參考通常是樣品溶解的物質。這兩束光都反射回探測器,但首先它們透過一個分離器,分離器快速交替使兩束光中的哪一束進入探測器。然後比較兩個訊號,並獲得列印輸出。
使用參考有兩個原因
- 這可以防止光源輸出的波動影響資料
- 這使得可以抵消溶劑的影響(參考通常是樣品所處溶劑的純淨形式)。
SDBS 是一個免費的線上光譜分析資料庫,包含許多紅外光譜、核磁共振光譜和質譜圖。