生物化學原理/酶
酶是有機催化劑,對所有生物體都很重要,因為細胞中不斷地進行著受控的化學活動。酶透過改變化學反應的速度來調節代謝。降低活化能是為了改變化學反應的速度。此外,酶能夠將一種形式的能量轉化為另一種形式的能量。由於酶具有高度選擇性,它們可能只催化一種或一類特定的反應。酶與底物結合的地方稱為活性位點。底物是酶作用的分子。
有兩種理論描述了酶的結合:1) 鎖鑰理論和 2) 誘導契合理論。
1) 鎖鑰理論:酶的活性位點的形狀與其底物的形狀互補。
2) 誘導契合理論:活性位點具有形狀的靈活性,因此當合適的底物與酶的活性位點接觸時,活性位點的形狀會發生改變以適應底物。
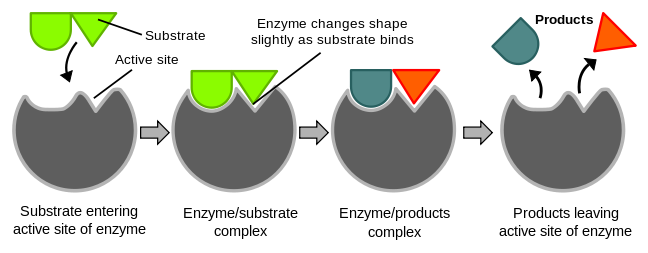
Figure 1 demonstrates the induced fit theory. Reference: en.Wikipedia, author: TimVickers
溫度
由於大多數酶反應是可逆的,因此酶可以合成和分解分子。酶反應速率取決於幾個因素:pH、溫度以及酶和底物的濃度。一般來說,酶反應速率隨著溫度的升高而增加;然而,如果達到最佳溫度 - 通常在 40°C 左右 - 酶會變性並失去與底物反應的能力。
pH
儘管每個酶都有自己的最佳 pH 值,但大多數酶反應在 pH 值 6 - 9 之間具有更高的反應速率。人體內酶反應的最大活性速率約為 pH 7.2,但胃蛋白酶除外,它在酸性條件下(通常約為 pH 2)具有較高的反應速率,胰腺酶在鹼性條件下(通常約為 pH 9)具有較高的反應速率。
濃度
此外,底物和酶的濃度也會影響反應速率。酶和底物的濃度越低,反應速度越慢,因為酶上的活性位點被佔用的越少。另一方面,酶和底物的濃度越高,反應速率越快,因為被佔用的活性位點更多。然而,一旦酶反應的反應速度達到一定程度,反應速率將不再增加。

圖 2 顯示了濃度與反應速率之間的關係。參考:en.Wikipedia,作者:fullofstars
酶抑制劑 酶抑制劑有兩類:1) 可逆抑制劑和 2) 不可逆抑制劑。可逆抑制劑在動力學上是可區分的,其特徵是酶抑制劑複合物迅速解離。
可逆抑制劑有三個子類別:1) 競爭性 2) 非競爭性 和 3) 非競爭性 競爭性抑制
雖然酶的活性位點具有高度特異性,但與底物形狀相似的分子有可能與活性位點結合。與分子結合的活性位點會干擾酶反應。因此,底物與活性位點結合的可能性更低,因此稱為競爭性抑制。然而,只有在分子和底物含量相似的情況下才會發生競爭性抑制。在競爭性抑制劑中,酶只能與底物或抑制劑結合,而不能同時結合兩者。此外,在競爭性抑制期間,底物的濃度會增加,而最大速度保持不變。

圖 3 展示了酶的競爭性抑制是如何工作的。參考:en.Wikipedia,作者:Jerry Crimson Mann,由 TimVickers 修改,由 Fvasconcellos 向量化。
非競爭性抑制 在非競爭性抑制中,抑制劑只與酶底物複合物結合。此外,在非競爭性抑制中,底物的濃度和最大速度都會降低。
非競爭性抑制
非競爭性抑制反應是不可逆的,因為分子與酶之間形成了不可透過新增過量底物來置換的強共價鍵。該分子也稱為非競爭性抑制劑。在非競爭性抑制中,抑制劑和底物可以同時在不同的結合位點與酶結合。此外,它可以結合遊離酶或酶底物複合物。此外,在非競爭性抑制期間,底物的濃度會增加,而最大速度會降低。
不可逆抑制劑有三個子類別:1) 基團特異性,2) 活性底物類似物,3) 機制依賴性抑制劑。基團特異性抑制劑只與氨基酸的特定側鏈或某些化學基團反應。
活性底物類似物,也稱為親和標記。在活性底物類似物中,分子在結構上類似於酶的底物,並共價結合到活性位點殘基。
機制依賴性抑制劑也稱為自殺抑制劑。該機制有三個步驟,第一步是氧化,然後是烷基化,最後是質子化。
輔因子
某些催化反應需要輔因子。輔因子可以是無機元素(金屬)或複雜的生物有機分子,其中許多來自維生素。全酶是指具有催化活性的酶;而脫輔酶是指沒有輔因子的酶。
吉布斯自由能 (ΔG)
酶降低活化能。酶透過降低過渡態的吉布斯自由能來加速反應,過渡態也稱為活化自由能。吉布斯自由能還提供了有關反應自發性的資訊。
反應是自發的,如果 : ΔG<0
反應是非自發的,如果 : ΔG > 0
反應處於平衡狀態,如果 : ΔG=0
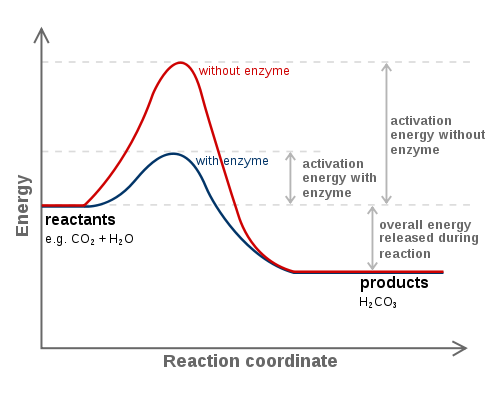 此圖顯示了酶的催化反應。參考:維基百科,作者:Fvasconcellos (talk · contribs)。
此圖顯示了酶的催化反應。參考:維基百科,作者:Fvasconcellos (talk · contribs)。
要確定反應的總吉布斯自由能,將產物的吉布斯自由能形成的總和減去反應物的吉布斯自由能形成的總和。關於 ΔG 的另一個重要點是,ΔG 無法解釋反應的反應速率。
Active Site
酶的活性位點是底物結合的地方,也是化學反應發生的地方。活性位點是蛋白質上的一個小部分,是一個裂縫或裂隙。它還具有獨特的微環境,底物透過多種弱相互作用結合。此外,酶的特異性取決於原子的精確排列。
生物化學反應
主要有兩種酶促反應:1) 順序反應和 2) 雙置換反應
1) 順序反應:在順序反應中,所有底物都在任何產物釋放之前與酶結合。在有序順序反應中,底物以確定的順序與酶結合;而在隨機順序反應中,底物以不確定的順序與酶結合。
2) 雙置換反應:在雙置換反應中,一種或多種產物在所有底物與酶結合之前被釋放。
- ↑ Kaplan PCAT 2010-2011 版
