氣體中的粒子由於彼此之間的碰撞而隨機地失去和獲得能量。 平均而言,對於大量的粒子,具有至少一定能量 ε 的粒子的比例是恆定的。 這被稱為玻爾茲曼因子。 它是一個介於 0 到 1 之間的值。 玻爾茲曼因子由以下公式給出
 ,
,
其中 n 是動能高於能量水平 ε 的粒子數量,n0 是氣體中粒子的總數,T 是氣體的溫度(以開爾文為單位),k 是玻爾茲曼常數(1.38 x 10−23 JK−1)。
這種能量可以是粒子可能具有的任何型別的能量 - 例如,它可以是重力勢能或動能。
在大氣中,粒子受到重力向下拉。 由於彼此之間的碰撞,它們獲得和失去重力勢能 (mgh)。 首先,讓我們考慮一小塊大氣。 它具有水平橫截面積 A,高度 dh,分子密度(每單位體積的分子數)n,並且所有分子都具有質量 m。 令塊中的粒子數為 N。

所以
 (如果你仔細想想,這是有道理的)
(如果你仔細想想,這是有道理的)
根據定義

總質量 Σ m 是單個分子的質量 (m) 乘以分子數量 (N)

然後計算塊的重量

向下的壓力 P 是每單位面積的力,因此

我們知道,當我們在大氣中上升時,壓力會下降。 因此,在我們的小塊中,存在由以下公式給出的壓力差 dP
 (1)換句話說,壓力正在下降 (-),它是這一小塊大氣重量的結果。
(1)換句話說,壓力正在下降 (-),它是這一小塊大氣重量的結果。
我們也知道

所以

但是

所以,透過替換

所以,對於我們的小塊
 (2)
(2)
如果我們將 (1) 和 (2) 等同

重新排列以獲得


在 n0 和 n 的極限之間積分
![{\displaystyle h={\frac {-kT}{mg}}\int _{n_{0}}^{n}{\frac {1}{n}}\;dn={\frac {-kT}{mg}}\left[\ln {n}\right]_{n_{0}}^{n}={\frac {-kT}{mg}}\left(\ln {n}-\ln {n_{0}}\right)={\frac {-kT}{mg}}\ln {\frac {n}{n_{0}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/56959ced2af27584ee8e2e47b7a9d9a4db5761b3)


由於我們正在處理重力勢能,ε = mgh,所以

此主題在 2010 年 6 月 Q10 494 中出現。該問題中使用的各種值的數值為

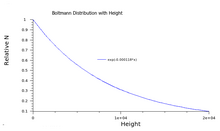 顯示如何透過高度獲得能量
顯示如何透過高度獲得能量
1u = 1.66 x 10−27 kg
g = 9.81 ms−2

1. 氮氣分子的分子量為 28u。如果地球大氣層是 100% 氮氣,溫度為 18 °C,那麼有多少比例的氮氣分子能達到 2 km 的高度?
2. 在 0 °C 下,一箱氫氣(分子量為 2u)中,有多少比例的分子速度大於 5ms−1?
3. 如果一半的氫氣以至少 10ms−1 的速度運動,那麼氫氣的溫度是多少?
4. 一些電離的氫氣(電荷 -1.6 x 10−19 C)放置在均勻的電場中。兩極板之間的電位差為 20V,兩極板之間的距離為 1m。在 350°K 的情況下,有多少比例的分子距離正極板至少 0.5m(忽略重力)?
解題步驟


















![{\displaystyle h={\frac {-kT}{mg}}\int _{n_{0}}^{n}{\frac {1}{n}}\;dn={\frac {-kT}{mg}}\left[\ln {n}\right]_{n_{0}}^{n}={\frac {-kT}{mg}}\left(\ln {n}-\ln {n_{0}}\right)={\frac {-kT}{mg}}\ln {\frac {n}{n_{0}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/56959ced2af27584ee8e2e47b7a9d9a4db5761b3)



