高階無機化學/烯烴複分解
烯烴複分解是一種有機化學反應,它利用金屬催化劑透過四元環中間體(也稱為Chauvin 機理)在烯烴(或烯烴)之間轉移取代基。這種有效的方法不僅產率高,而且與其他有機反應相比,副產物和有害廢物更少。伊夫·肖萬、羅伯特·H·格拉布斯和理查德·R·施羅克因其對烯烴複分解的貢獻而獲得了 2005 年諾貝爾化學獎。
20 世紀 50 年代,工業化學家赫伯特·S·埃盧特里奧在他的一項實驗中發現,在 Mo-Al 催化劑上,從丙烯原料中得到了丙烯-乙烯共聚物。他重複了用環戊烯的實驗,並注意到“聚合物看起來像有人拿著一把剪刀,打開了環戊烯,然後整齊地縫合了它”。其他化學家也得到了類似的結果,即烯烴雙鍵的斷裂和重新形成。格拉布斯認為,取代基的重排是透過金屬環戊烷中間體發生的。肖萬提出,烯烴複分解是由金屬卡賓引發的。許多科學家同意肖萬的觀點,即金屬卡賓在烯烴複分解過程中起著主要作用,從那時起,人們對其進行了更深入的研究,以瞭解完整的機理。
兩個烯烴上取代基的重排是透過形成一個四元環中間體發生的,如下圖所示。
具有取代基 R1 的初始烯烴與烯烴金屬卡賓形成中間體,使金屬元素與初始烯烴連線。然後,產物與具有取代基 R2 的第二烯烴反應,形成另一個四元環中間體,併產生具有 R1 和 R2 兩種取代基的最終組合烯烴,同時產生初始金屬卡賓。這種型別的四元環形成被稱為 [2+2] 環加成。四元環不是最穩定的,已知會導致分子應力。結果,形成具有非常高的活化能。與金屬的相互作用降低了環形成的活化能,使過程能夠在中等溫度下發生。
烯烴複分解需要使用金屬催化劑。最常用的催化劑是格拉布斯催化劑和施羅克催化劑。
格拉布斯催化劑是一種市售的催化劑,易於操作,因為它對水、氧氣和其他少量雜質非常穩定。雖然它具有高官能團耐受性等優點,但也存在缺點,即與其他催化劑(如 Mo 亞胺烷烴催化劑)相比,其反應活性較低。
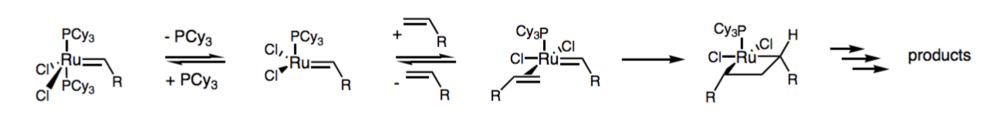
與烯烴相互作用後,會形成一個與卡賓順式且與 Cl 原子反式的四元環。

與格拉布斯催化劑類似,施羅克催化劑也是市售的。它比格拉布斯催化劑具有更高的反應活性,並且可以耐受多種官能團,但它也存在許多缺點,例如需要在惰性氣氛下使用乾燥的溶劑和底物進行操作,並且不能耐受雜原子上的質子。
- 開環複分解聚合 (ROMP)
- 閉環複分解 (RCM)
- 交叉複分解 (CM)
- 非環二烯複分解聚合 (ADMET)
烯烴複分解為石油化工、聚合物以及更多領域開闢了新的工業途徑。在石油化工領域,烯烴複分解用於烯烴轉化技術 (OCT) 工藝和殼牌高階烯烴工藝 (SHOP)。ROMP 為在許多工業方法中生成具有特殊效能的有用聚合物提供了機會。為了未來的油化工進展,天然脂肪的複分解為可能提供了可能性。目前,最重要的應用是生產丙烯、洗滌劑級烯烴和聚合物。
- Jen, W. "有機合成中的烯烴複分解".
{{cite journal}}: Cite journal requires|journal=(help) - Mol, J.C. "烯烴複分解的工業應用". 213 (1): 39–45. doi:10.1016/j.molcata.2003.10.049.
{{cite journal}}: Cite journal requires|journal=(help) - Rouhi, A.M. "烯烴複分解:早期". 80 (51): 34–38.
{{cite journal}}: Cite journal requires|journal=(help)
