數字放射成像基礎物理學/影像接收器

本章描述了數字放射成像影像接收器的技術方面。這些接收器通常用於放射成像,有些也可以用於透視成像。因此,除了單次曝光放射成像之外,其他曝光模式也可以與所述技術一起使用。透視成像中連續 X 射線曝光的使用通常是指使用低 XRT 電流(即 0.5 到 5 mA)——參見圖 4.1。所得影像的影像質量較低,但足以用於患者定位或監測 導管 置入。其使用也被稱為透視,這是指過去使用塗有熒光材料的玻璃板進行這種成像的日子。相反,透視攝影通常是指使用相對強烈的(例如 50 到 1000 mA)脈衝曝光。脈衝通常持續時間很短,並且可以以例如每秒 1 到 8 次的速率施加。所得影像具有相對較高的影像質量,因此可以用於診斷目的。
我們之前描述過 光激發發光 的過程,該過程在計算機放射成像中得到利用,其中輻射的吸收導致電子被捕獲在中間能級。具有此特性的磷光體因此被稱為儲存磷光體。
可以使用塗有 晶體 的鋇氟鹵化物化合物(其中包含微量的 銪)的板記錄潛像。這些化合物的通式為 BaFlX:Eu,其中 X 可以是 Cl、Br 或 I 或它們的混合物。放射成像資訊透過將電子提升到能隙中的陷阱來記錄,填充陷阱的數量與吸收的輻射能量量成正比。當受到約 600 到 680 奈米(即紅光)波長的可見光刺激時,晶體發光,因為電子返回到 300-500 奈米(藍色)範圍內的基態。

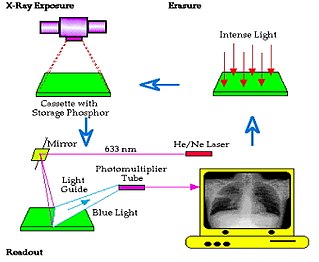
- 該板可以用細聚焦的 雷射 光束(例如 He/Ne)和掃描鏡以 光柵模式 掃描——參見圖 4.2。雷射光刺激從陷阱中釋放電子,從而產生光發射,該光發射由光導收集並饋送到 光電探測器(例如,光電倍增管)。當板被掃描時,光電探測器產生的訊號被放大並由 模數轉換器 (ADC) 數字化。
- 該影像本質上逐點逐行構建,從而提供高達 4k x 4k 畫素 的數字影像解析度。畫素大小通常為 0.1 μm。成像迴圈透過用高強度 鈉蒸汽燈 照射板來完成,該燈擦除潛像的任何殘留物,並且基本上為板準備重複使用——參見圖 4.3。
- 計算機放射成像的空間解析度受諸如磷光板厚度、讀出時間和雷射束直徑等因素的影響,雷射束直徑通常約為 100 μm。注意,雷射光在磷光層主體中的散射會使受激區域的寬度超出該直徑。
- 注意,CR 成像過程的性質限制了其在單次曝光放射成像中的應用。在臨床實踐中,該過程通常是工作流程的一部分,其中患者放射照片像傳統膠片/增感屏放射照片一樣被記錄下來,但現在影像是在潛像讀出裝置上生成的,並自動傳送到質量控制工作站進行影像評估、註釋和傳輸到 PACS 用於報告。

- CR 成像板在結構上與增感屏非常相似。它由嵌入有機粘合劑中的約 5 μm 的微小磷光顆粒組成,這些顆粒塗覆在基底材料上。該板是不透明的,因此強烈且各向同性地散射光(激發雷射和受雷射)——參見圖 4.4。因此,光擴散限制了磷光層的有用厚度。透過增加磷光層厚度,確實可以提高 X 射線吸收效率。但是,
- 磷光層中光的橫向擴散將與層厚度成正比增加,從而損害空間解析度;並且
- 當層超過一定厚度時,靈敏度不會顯著提高,因為大部分在層深處激發的光將無法到達表面以供檢測。
- 透過使成像板的基底由透明材料製成並從板的正面和背面檢測光激發發光[1],可以克服這種靈敏度限制。這需要兩個光收集系統,但只需要一個雷射束。改進的靈敏度是由於使用傳統的單雷射方法僅收集了約 30% 的光激發光。此外,使用結構化磷光體(例如,CsBr:Eu——參見 下面的討論)作為成像板[2],已經實現了靈敏度的提高。
CR 的一個基本限制是讀取潛像所需的時間。由於磷光發光的衰減時間通常約為 0.7 μs,因此讀取 3,000x3,000 畫素的影像可能需要超過半分鐘才能完成。可以透過線掃描來獲得改進,其中一整行的畫素同時被激發和讀出,而不是像上面描述的那樣逐個畫素進行。這種線掃描方法需要線性排列的雷射光源(例如,雷射二極體),以及與成像板一樣寬的線性排列的光電探測器,並且會產生小於 10 秒的讀出時間。此外,線性掃描機制可以內建到影像接收器盒中[3]。
注意,已經發現使用 CR 板進行臨床放射成像會產生一系列獨特的偽影,這些偽影在 Cesar 等人的一篇圖片評論中進行了介紹。(2001)[4]。

近年來,在數字放射成像的平板影像接收器的開發方面進行了大量研究。這項研究已經擴充套件到開發用於例如筆記型電腦的主動矩陣液晶平板顯示器(AMLCD)。AMLCD 的基礎技術是一種稱為主動矩陣陣列的大面積積體電路,它由數百萬個相同的半導體元件組成,這些元件沉積在基材材料上。與這種主動矩陣陣列耦合的增感屏或光電導體構成了平板 X 射線影像接收器的基礎。這些探測器已應用於放射成像和透視成像。
這種接收器如圖 4.5 所示,其中主動矩陣陣列和相關電子電路安裝在盒式磁帶中。陣列尺寸可達 43 釐米 x 43 釐米,擁有超過 900 萬個畫素(畫素尺寸約為 140 μm)。陣列的操作由數字影像處理器控制(見下一章),它還儲存和顯示生成的影像。
圖 4.6 說明了操作的簡化描述。陣列的每個畫素都帶有一個開關(通常由薄膜晶體管制成),該開關以允許同時操作陣列中一行中的所有開關的方式連線到切換控制電路。每個畫素的輸出與單個前置放大器按列連線。在 X 射線曝光期間,所有開關均保持關閉狀態。曝光後,第一行的開關開啟,每個畫素的訊號由前置放大器放大,使用 ADC 進行數字化並存儲在數字影像處理器的影像儲存器中。然後關閉這些開關,並開啟第二行的開關以獲取來自第二行畫素的訊號。此過程對整個陣列重複,因此以順序的逐行方式獲取影像。當接收器用於透視成像時,陣列會連續掃描[5]

研究開發已在兩個方面取得進展,如圖 4.7 所示。
間接接收器
[edit | edit source]- 間接接收器基於將增感屏耦合到主動矩陣陣列。已使用 Gd2O2S:Tb 和 CsI:Tl 等磷光體,並且在 X 射線相互作用後產生的光被由光電探測器組成的畫素陣列檢測 - 見圖中的面板 (a)。每個光電探測器都會產生與照射到它的光量成正比的電荷,並且該電荷會儲存起來,直到它被切換控制電路讀出。由於檢測到的 X 射線首先被轉換為光,然後被轉換為電荷,因此該檢測過程稱為間接檢測。
- CsI:Tl 作為增感屏具有明顯的優勢,因為它在 33 keV (I) 和 36 keV (Cs) 處具有良好的 K 吸收邊,並且其晶體可以在高達 600 μm 厚度的薄層中以密集的針狀(直徑 5-10 μm)結構生長[6]。因此,由 X 射線吸收產生的熒光可以透過光纖引導到光電探測器陣列,而不會產生太多橫向色散。因此,CsI:Tl 是一種所謂的結構化磷光體,與使用 Gd2O2S:Tb 和類似螢幕獲得的分散粉末磷光體形成對比。由於其晶體結構,CsI:Tl 中閃爍點的堆積密度也非常高,而粉末螢幕僅包含約 60% 的磷光體和 40% 的粘合劑。這使得結構化磷光體的吸收效率比具有類似空間解析度能力的粉末螢幕高約四倍。
- CsI:Tl 在可見光譜的綠色區域發出熒光,在那裡 a-Si 的光吸收效率相對較高。
- 間接接收器也已應用於計算機斷層掃描。例如,在 MDCT 中,由磷光材料製成的多達 916 列 x 64 行的探測器元件陣列與 a-Si 光電二極體陣列耦合。超快陶瓷 (UFC) 探測器,以摻雜的硫氧化釓晶體制造,具有相對快速的響應、高檢測效率和寬動態範圍。此外,可以將準直器葉片直接安裝在探測器陣列上以降低散射。
直接接收器
[edit | edit source]- 直接接收器基於將光電導體耦合到主動矩陣陣列。已使用無定形硒 (a-Se) 等光電導體,並且在 X 射線相互作用後產生的電荷被由電極和電容器組成的畫素陣列檢測 - 見面板 (b)。該電荷儲存在每個電容器中,直到它被電子切換電路讀出。光電導體需要使用表面電極施加大約 5,000 伏的電壓,以便產生的電荷可以被吸引到畫素電極。
- 硒作為 X 射線吸收材料的效率不如碘化銫,因為它的原子序數 (Z=34) 較低。它的 K 吸收邊在 13 keV,並且其衰減隨著能量的增加而迅速下降。在此基礎上,可以預期需要相當厚的 a-Se 層才能以與 CsI 在較高 X 射線能量下相同的效率吸收 X 射線光子。其他潛在材料,如氧化鉛 (PbO)、碘化鉛 (PbI2) 和碘化汞 (HgI2) 存在,它們對給定層厚的吸收效率優於硒,並且可能在未來得到應用[7]。
平板影像接收器的重要設計特徵包括畫素尺寸和填充率。畫素尺寸影響空間解析度,典型的尺寸約為 100-200 μm。填充率是指對影像訊號(無論是電荷還是光子)敏感的畫素區域的百分比。鑑於需要容納輸入切換訊號的導體(約 10 μm 寬)和輸出影像訊號的導體,以及每個畫素中的薄膜電晶體,它永遠不會達到 100%。典型的填充率在 50-80% 的範圍內。
平板探測器通常使用氫化的無定形矽 (a-Si:H+) 的主動矩陣作為讀出陣列。這是為筆記型電腦顯示器開發的技術,它使製造具有高輻射耐受性的超大面積 X 射線成像器成為可能。例如,無定形矽層透過等離子體增強沉積矽烷 (SiH4) 氣體在玻璃基板上形成。無定形層的無序結構的優點是,X 射線檢測可以在沒有輻射損傷材料的情況下進行。因此,該材料可以重複暴露於相對強烈的 X 射線束中。主動矩陣陣列透過光刻和化學蝕刻技術從 a-Si 層製造,這些技術廣泛應用於積體電路製造。
但是,a-Si 受限於可以構建到該材料中的結構的最小尺寸。另一種可能性是基於互補金氧半導體 (CMOS) 技術的讀出陣列。CMOS 使用晶體矽晶片而不是無定形矽製成,並且在半導體行業高度發達。CMOS 成像器提供高填充率和非常快速的讀出。此外,可以為每個畫素整合片上電子器件(例如放大器),這可以顯著提高效能,並且有一天可能會提供 X 射線能量辨別能力。但是,由於存在明顯的電子噪聲,它們在 DR 中的使用受到限制。
間接探測器設計的變體是在增感屏的前側安裝光電二極體/TFT 陣列 - 稱為輻照側取樣 (ISS)[8]。這裡的優勢在於改善了螢幕中閃爍點與光電二極體之間的檢測幾何形狀,從而減少了光衰減和模糊效應。
可以使用間接和直接影像接收器的特徵獲得一種有趣的混合設計。在這裡,結構化磷光體與薄 a-Se 層耦合,並且當使用可程式設計施加電壓控制電子放大時,具有潛在的優勢。
使用直接探測器的光學讀出可以減少TFT和相關電路產生的電子噪聲。這裡使用兩層a-Se,中間隔著一層電子俘獲層(ETL)。一層在吸收X射線時產生電子,這些電子被ETL俘獲,第二層較薄的層在被一行掃描的LED陣列照射時用於讀取該電荷[9]。

圖 4.8 顯示了X射線影像增強器 (XII) 和影片系統的基本元件。從患者體內射出的X射線在 XII 中被轉換為光學影像,該影像被 攝像機 觀看並使用計算機系統顯示。這些系統廣泛用於 透視 和 熒光造影,在 鋇餐檢查、血管造影 和 介入放射學 中。它們的歷史發展在 Balter (2019) 中進行了回顧[10]。
許多系統還具有在 XII 輸入端放置 CR 或 DR 盒的機制,以便可以記錄放射影像。此裝置有時被稱為盒式轉換器,可以允許將多個影像記錄到一個影像接收器上。包含盒式轉換器的單元有時被稱為放射攝影/透視 (R/F) 系統 - 請參見圖 4.9。

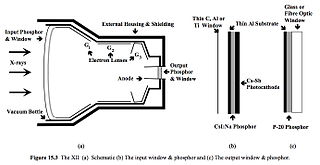
- 圖 4.10 說明了 X射線影像增強器的基本特徵。X射線束從患者體內射出後,進入 XII 管,被輸入 熒光粉 吸收,從而產生光子。這些光子撞擊 光電陰極,使其發射電子。電子被陽極和光電陰極之間產生的高電場加速朝向輸出熒光粉移動。聚焦由聚焦透鏡完成。電子撞擊輸出熒光粉,產生大量光子,這些光子攜帶透檢視像。透過這種複雜的方式(參見圖 4.11),XII 將 X射線影像轉換為電光增強的光影像。
- 影像增強也來自於輸出熒光粉遠小於輸入熒光粉。輸出熒光粉的直徑通常約為 2 釐米,而輸入熒光粉的直徑可能因臨床應用而異,從約 15 釐米到 40 釐米不等。因此,影像縮小帶來的增強倍數可能在 56 到 400 之間。透過管內的電子加速(即通量增益)可以實現額外的增強。獲得的總亮度增益(即縮小倍數乘以通量增益)可以超過 5,000[11]。
- 輸入視窗通常由一層薄薄的 鈦、碳纖維 或 鋁 製成,以最大程度地減少 X射線的吸收。輸入熒光粉通常是摻鈉的碘化銫 (CsI:Na)。輸入熒光粉和光電陰極必須緊密接觸以保持潛像保真度 - 請參見面板 (b)。電子以與輸入熒光粉亮度成正比的方式產生,並被加速透過 25-35 kV 的電位,然後撞擊輸出熒光粉。這個加速陽極位於抽真空管的頸部。
- 靜電聚焦透鏡 (G1、G2 和 G3) 相對於陰極具有正電位。光電陰極實際上是彎曲的(與圖 4.10 中顯示的不同),以使所有電子的路徑長度相等,從而最大程度地減少影像失真。

- 輸出熒光粉通常由一種稱為 P20 的熒光粉製成。這種熒光粉發出綠光,與攝像機的靈敏度非常匹配。在該輸出熒光粉上鍍上一層非常薄的鋁,以防止光線反射回管內並激活光電陰極 - 請參見面板 (c)。這層也作為 接地,用於從管中去除用過的電子。
- 玻璃外殼包裹在一個鉛襯套中,該襯套提供一定程度的輻射防護,防止 X射線散射。還加入了外部磁場的防護。許多 XII 設計還在輸入端加入了一個固定式放射攝影柵格。
- 可以透過改變圖 4.10 中所示靜電透鏡 G3 上的電壓來實現可變場大小。增加該電壓可以用來減少可以在輸出熒光粉上成像的輸入熒光粉的區域,但它也會降低縮小增益。通常需要增加輻射照射量(即 mA)來進行補償。在介入放射學等需要精細控制的情況下,這種可變場大小很有用。但是,應該理解,當需要等亮度的影像時,由此產生的患者照射量變化與場大小的平方成反比。
- 應該理解,即使具有相當大的亮度增益,輸出熒光粉上的影像仍然非常暗淡,無法直接觀看。這就是通常使用攝像機來觀看 XII 輸出的原因之一。此外,應該理解,XII 影像會受到枕形失真和漸暈等效應的影響。
- 攝像機透過光學耦合觀看 XII 的輸出,光學耦合由一個簡單的透鏡系統和一個光圈組成。光圈可以用來控制照射到攝像機的光量。或者,攝像機和 XII 可以透過光纖光學耦合。
- 透視中使用兩種主要型別的攝像機。傳統裝置稱為 光電導攝像機 或拾取管 (PUT),如圖所示,以及更近期的半導體或 CCD 攝像機。兩種攝像機都以影片訊號的形式生成影像,但方式大不相同。下面描述了這些攝像機的操作。
- 光電導攝像機
- PUT 攝像機使用一種稱為 靶 的光敏感測器。XII 的輸出影像聚焦到靶元件上(參見圖 4.12),靶元件由三層夾層組成。第一層是玻璃面板,它只用於保持真空,同時傳輸入射光。接下來是信號板,它由一層薄薄的透明導電石墨膜組成。約 40 伏的電位施加到這層。夾層的第三個成員是靶,它是一層薄薄的光電導材料膜。

- 攝像機的一個重要部分是真空管,其長度通常高達 15 釐米,直徑高達 3 釐米。它可以被聚焦和偏轉電子束的線圈包圍。或者,稱為偏轉器的偏轉電極可以被塑造成真空管內壁的形狀。
- 管子的另一端是陰極。透過間接加熱,電子從陰極表面沸騰出來,並被高達 900 伏的電壓加速到陽極。陽極以細金屬網的形式延伸到管子末端,允許大部分電子束穿過它。一旦穿過,它們就會減速撞擊信號板。電子束使用聚焦線圈聚焦到一個微小的點,聚焦線圈幾乎延伸到管子的整個長度。聚焦的電子束可以透過對偏轉器施加合適的電壓來進行垂直和水平偏轉。
- 照射到光電導靶上的光會改變其電導率,變化的程度與光強成正比,這些變化由掃描電子束讀取。產生的電流透過透明導電膜傳送到外部電路,在那裡可以開發出 影片電壓。
- 半導體攝像機

- 請注意,CCD 攝像機也已在放射學應用中直接觀察增感屏中得到應用[12]。

- 攝像機控制單元提供攝像機與顯示器之間的連線。它包含一個 振盪器 電路,例如,用於控制 PUT 攝像機的電子束偏轉,或控制 CCD 攝像機的隔行傳輸,並將錄製影像與影片監視器上顯示的影像或儲存在計算機記憶體中的影像同步。同步通常使用在每行影片和幀的 消隱間隔 期間插入的 同步脈衝 來實現 - 見圖 4.14。控制單元中的主放大器調整影片放大器的增益,以便影片訊號範圍(通常為 0 到 1 伏)可以得到充分利用。此功能稱為 自動增益控制 (AGC)。
- 請注意,影片影像通常是矩形的。影像寬度與高度的比率稱為 縱橫比,通常為 4:3。這並不理想地適用於醫療成像,其中攝像機正在觀看 XII 生成的圓形影像。
自動亮度控制
[edit | edit source]- 在透視成像中遇到的身體部位厚度和成分範圍相當大。例如,在鋇上消化道檢查中,從篩選頸部到篩選胃部會大大增加沿途的 X 射線衰減,並導致影像變暗,除非調整曝光因素和/或攝像機的增益以進行補償。曝光因素的調整通常稱為自動亮度控制 (ABC),而基於攝像機的調整由上述 AGC 提供。ABC 用於在檢查過程中保持顯示影像的亮度處於恆定水平。它涉及根據所檢查的解剖部位自動調整 kV 和 mA。例如,這可以透過 XII 輸出處的小型光電感測器來實現,該感測器監控增強的影像的中心部分並將訊號反饋到發生器以相應地調整 kV、mA(或兩者)。
- ABC 系統通常設計為在最小 (例如 70 kV) 和最大 (例如 120 kV) 千伏電壓之間執行。例如,可以在曝光序列開始時使用最小 kV 來防止低能 X 射線不必要地照射患者,然後自動增加 kV 以達到預定的影像亮度水平。在該過程中,管電流 (mA) 也可以自動調整。在 ABC 的 kV 範圍內,這種 mA 調整受到 XRT 的功率額定的限制。當達到功率限制時,例如,在腹部側面的透視或在傾斜角度的心臟投影中,曝光因素的進一步調整不再可能,AGC 電路可以發揮作用以保持影像亮度。但是,影像通常會產生更高的電子噪聲。
- ABC 系統使用的實際 kV 和 mA 設定決定了透檢視像中顯示的對比度以及患者的劑量。可以使用高劑量 ABC 模式,該模式會降低 kV 並提高 mA,以便在相同影像亮度下可以提高影像對比度,而低劑量模式會提高 kV 並降低 mA 以實現類似的結果。許多系統上還可以選擇第三種中間模式。XRT 的熱容量施加了功率限制,該限制由乘積 (kV x mA) 控制,ABC 系統會自動應用。這由所篩選解剖部位的厚度和成分決定。當該乘積達到功率限制時,例如,對於非常大的患者,ABC 通常會保持恆定的 kV 和 mA 設定。因此需要攝像機的 AGC 提供的額外控制。此外,AGC 對影像亮度的控制幾乎是瞬時的,而高壓電路可能需要大約一秒鐘才能響應任何 ABC 檢測到的照度變化。因此,AGC 在此適應期內也很有用,以便在顯示的影像中保持恆定的亮度。
輻射劑量管理
[edit | edit source]許多系統上都提供了一個指示生成 CR 或 DR 影像所需的輻射照射量的指標。該指標可以稱為靈敏度指數 (SI)、對數中值 (LgM)、曝光指數 (EI) 或類似引數,可用於衡量曝光的充分性。請注意,這些引數通常參考在特定條件下(例如 X 射線能量、束過濾等)生成的曝光,因此只能被視為患者劑量的粗略指標。
劑量面積積 (DAP) - 請參見 下面的討論 - 記錄可用於回顧臨床環境中隨時間的曝光趨勢[13]。這裡的目標之一是減少曝光爬升現象,在這種現象中,例如,為了追求優質影像,曝光會隨著時間的推移而緩慢增加。這裡的另一個目標可以是檢視相對於 診斷參考水平 (DRLs) 的曝光測量值。
重複曝光分析也可以與這種曝光回顧相結合,以便例如,X 射線工作人員團隊可以共同努力提高工作效率。重複拍攝的理由可以歸類為放射學曝光錯誤,包括因患者移動而導致的錯誤(例如,使用時間過長的曝光),以及放射學定位錯誤[14]。
- 近年來,隨著大量關於脫髮和皮膚損傷的報告,人們對減少透視劑量產生了濃厚的興趣。這些損傷是由於患者接受長時間介入手術造成的[15]。世界各地的監管機構已對國際放射防護委員會的討論作出回應[16],併發布了以下建議,建議裝置負責人
- 研究發現,皮膚損傷對以下因素很敏感:之前的過量輻射暴露、藥物、結締組織疾病和糖尿病。Balter 等人 (2010) 對頭髮和皮膚影響進行了綜述[17]。例如,介入放射學中單部位皮膚劑量超過 2 Gy 會導致紅斑和脫髮,劑量更高則會導致永久性皮膚損傷。
- 已開發的減少患者劑量的機制包括
- 準直:由於傳統的矩形準直器與基於 XII 的透視系統(產生圓形影像)一起使用會導致未使用的曝光,因此一些現代系統使用圓形準直器。這些準直器通常具有自動響應源到影像距離變化和 XII 中使用的電子縮放選擇的功能。這樣會形成一個複雜的準直器元件,該元件基於可調節的多葉吸收器,並且可以包括機器人控制。這方面另一個功能被稱為無輻射準直器定位,它涉及將影像儲存在計算機記憶體中,停止曝光並調整準直器控制裝置,以便計算機生成準直區域的圖形顯示。
- 數字影像儲存:由於影像儲存在計算機記憶體中(請參見下一章計算機),因此可以實現以下功能:最後影像保持 (LIH),即不斷顯示最近獲取的影像,而不照射患者,參考成像,即將先前獲取的影像顯示在第二個影片監視器上以進行比較,影像瀏覽,即可以顯示先前獲取的多個影像,以及透視迴圈,即可以連續回放成像序列以進行更仔細的檢查。
- 自動亮度控制 (ABC) 可以與曝光脈衝控制和附加濾波器結合使用,從而產生所謂的自動劑量率控制 (ADRC)[18]。在此,可以根據篩查開始時遇到的特定曝光因素,自動選擇不同的濾波器插入 X 射線束。例如,一些 ADRC 系統可以產生以下選擇
- 在成像序列期間保持恆定的電壓,
- 保持影像亮度的 mA 脈衝高度和寬度,以及
- 自動插入不同厚度的銅濾波器,
- 這取決於待檢查身體部位的厚度和成分。例如,此類系統可以使用四個可選銅濾波器,其厚度分別為 0.2、0.3、0.6 和 0.9 毫米,具體取決於患者的厚度。由於吸收劑量對於較厚的患者而言更大,因為需要更高的曝光因素才能獲得亮度足夠的影像,因此會選擇一個能夠適當地硬化 X 射線束並減少患者劑量的濾波器厚度。這被稱為光譜濾波。ADRC 系統可以使高壓發生器根據銅濾波器厚度選擇恆定 kV,並根據解剖結構改變 mA 脈衝高度。例如,它可能為腳等薄身體部位選擇 60 kV 和 0.9 毫米銅濾波器,而為厚度大於 20 釐米的身體部位選擇 80 kV 和 0.3 銅濾波器,並透過生成必要強度的脈衝來調整每次曝光的 mA。
- 大多數透視系統還具有聲音警報功能,在“束開啟”時間達到五分鐘後會發出警報。累積曝光時間通常會即時顯示在影像顯示器上,以及 kV 和 mA - 以及在安裝了劑量面積積量計 (見下文) 時顯示劑量率讀數。
- 工作人員在操作放射照相和透視裝置時,會受到三種輻射源的照射:用於照射患者的初級射線束、來自 XRT 的漏射線以及來自患者的散射線。在工作人員需要在曝光期間留在 X 射線室或手術室的情況下,可以穿戴鉛圍裙並利用距離來最大程度地減少漏射線和散射線的影響。但是請注意,鉛圍裙的 X 射線衰減率僅約為 90-95%,具體取決於鉛當量。這些圍裙通常由含鉛乙烯基製成,相當於 0.25-0.5 毫米鉛,重量約為 5 公斤。用鎢和錫等複合材料製成的具有類似衰減率的更輕便的圍裙可能對長時間進行介入手術的工作人員很有用。在曝光期間,與患者近距離接觸的工作人員應使用 0.5 毫米鉛當量的圍裙。與無背部設計的圍裙相比,更安全的款式是環繞式圍裙。從實際角度來看,鉛圍裙應始終垂直儲存在架子上,因為摺疊會造成裂縫,從而降低其有效性。此外,鉛圍裙應每年至少進行一次放射照相檢查,以檢查是否有任何磨損或損壞跡象。
- 此外,可以將患者附近工作人員的人數降至最低,並在即將曝光時發出警告。理想情況下,工作人員應在曝光期間位於遮蔽的操作員控制檯區域後面。X 射線室的設計使得通常可以透過充分的遮蔽和距離來確保最佳化房間內任何人員(控制檯後方或房間外部)的劑量。
- 在一些介入性情況下,介入醫師可能發現有必要在部分手術過程中將手放在主射束中。這種多年來的反覆暴露可能會最終導致放射性皮炎。在這種情況下,可以透過調整成像系統使手保持在患者的射束出口側來實現劑量最佳化。例如,如果 XRT 位於患者下方,則操作導管的手應該位於患者上方。

- 還應注意,在透視中使用床上式 XRT 會導致工作人員劑量明顯高於使用床下式 XRT 的系統 - 見圖 4.15。患者散射的輻射增加以及患者床結構提供的遮蔽不足是原因。例如,在使用床上式系統而沒有防護屏的放射科醫生中,發現鏡頭損傷發生率增加[19]。然而,請注意,當使用倒置 C 型臂來輔助手部手術時,這種床上式論點可能並不總是有效[20]。

- 在心臟導管室、手術室和血管造影室中使用 C 型臂和類似的裝置會帶來額外的危害 - 見圖 4.16。這些危害的出現是因為使用鉛遮蔽裝置的人體工程學問題 - 這些裝置旨在最大限度地減少介入醫師位置處的散射和洩漏。因此,他們的甲狀腺和眼晶狀體可能會接受大量的劑量。在這種情況下,可以佩戴甲狀腺遮蔽和鉛眼鏡,並使用可調節的鉛玻璃遮蔽來最佳化劑量[23][24]。一般來說,眼鏡也需要側面保護,遮蔽相當於 0.25 毫米的鉛。此外,介入醫師可以在頸部佩戴第二個劑量計,以監測他們甲狀腺和眼睛的劑量。請注意,在心臟導管室工作人員(包括醫務人員和臨床人員)的眼中觀察到與輻射相關的後晶狀體變化 - 其中大多數人沒有佩戴鉛眼鏡 - 其發生率明顯高於未暴露的對照組[25],並且一項針對大量介入心臟病學家的白內障發生率研究已經啟動[26]。
- 介入醫師在手術過程中的位置對他們的手部劑量有很大影響[27]。可以使用靠近 XRT 的手指上的環形劑量計來監測此類劑量。通常不佩戴鉛手套,原因是人體工程學因素,以及因為當遮蔽的手在射束中時產生的額外衰減會增加自動控制的曝光因素。請注意,在泌尿外科[28]和血管內手術[29]等專業領域可能需要特別的額外最佳化技術。
患者劑量
[edit | edit source]- 應使用良好的成像幾何形狀來最佳化放射學、透視和熒光攝影中的患者防護。在大多數情況下,影像接收器應因此移至距 XRT 最遠的位置,並將患者儘可能靠近影像接收器。換句話說,患者應該理想地移動到影像接收器,而不是反過來。一些透視系統可以自動執行此操作,以便在曝光之前在患者和影像接收器之間保持狹窄的空氣隙。
- 可以預期,患者接受透視手術的有效劑量明顯高於普通放射學 - 見下表。較高的劑量來自透視篩選曝光和多次熒光攝影曝光。請注意,身體中包含許多放射敏感器官(如腹部)的強衰減部位會在表中產生較大的劑量。
| 程式 | 有效劑量 (mSv) |
|---|---|
| 腦血管造影 | 2.5
|
| 腎造瘻術 | 5.5
|
| 鋇餐 | 8.2
|
| 腎動脈造影 | 10.3
|
| 鋇灌腸 | 11.7
|
| 膽道支架置入術 | 12.5
|
| 腸造影 | 14.0
|
- 可以從表中看出,所有劑量都高於平均年度背景劑量 (2.4 mSv)。從這個角度來看,腦血管造影的劑量相當於大約 1 年的背景暴露 - 其所謂的背景輻射等效時間 (BERT)。但是請注意,由於患者解剖結構差異和成像技術質量等因素,患者劑量測定調查資料可能會存在相當大的變化,變化幅度可能超過 10 倍。還要注意,世界不同地區背景暴露的變化幅度可能超過 100 倍。很明顯,BERT 只是一個非常近似的相對劑量指標。
- 上表中較高的劑量,以及在延長介入手術中更高的劑量,促使人們使用劑量測定裝置來常規監測劑量面積積 (DAP) 和峰值皮膚劑量等引數。DAP(也稱為克爾瑪面積積)是衡量 XRT 出射總能量的指標,通常在靠近準直器的射束中某個位置測量(以 Gy cm2 為單位)。該引數的優點是它獨立於源到皮膚距離,如之前所述,可用於估計手術的隨機風險。峰值皮膚劑量是確定確定性效應可能性的一種有用指標。此類測量也可用於建立劑量刻度,以幫助介入人員進行輻射劑量管理[36]。
| 模態 | 檢查 | 平均有效劑量 (mSv) |
|---|---|---|
| 普通放射學 | 四肢 | 0.001 |
| 膝蓋 | 0.005 | |
| 肩膀 | 0.01 | |
| 胸部 (PA) | 0.02 | |
| 胸部 (PA + 側位) | 0.1 | |
| 頭骨 | 0.1 | |
| 頸椎 | 0.2 | |
| 乳腺X線攝影 | 0.04 | |
| 骨盆 | 0.6 | |
| 腹部 | 0.7 | |
| 髖部 | 0.7 | |
| 胸椎 | 1 | |
| 腰椎 | 1.5 | |
| 靜脈腎盂造影 | 3 | |
| DEXA | 無 CT | 0.001 |
| 帶 CT | 0.04 | |
| 透視 | ERCP | 4 |
| 小腸系列 | 5 | |
| 上消化道系列 | 6 | |
| 鋇灌腸 | 8 | |
| 計算機斷層掃描 | 頭部 | 2 |
| 頸部 | 3 | |
| 鈣化評分 | 3 | |
| 骨盆 | 6 | |
| 脊柱 | 6 | |
| 胸部 | 7 | |
| 腹部 | 8 | |
| 虛擬結腸鏡檢查 | 10 | |
| CTPA | 15 | |
| 三相肝臟 | 15 | |
| 冠狀動脈造影 | 16 | |
| 介入放射學 | 頭頸部血管造影 | 5 |
| 胸部血管造影 | 5 | |
| 冠狀動脈造影 | 7 | |
| 腹部血管造影 | 12 | |
| CTPA、支架或射頻消融 | 15 | |
| 盆腔靜脈栓塞術 | 60 | |
| TIPS 置入術 | 70 | |
| 牙科放射學 | 口腔內放射學 | 0.005 |
| 全景放射學 | 0.01 | |
| 牙科 CT | 0.2 |
下面顯示了此資料的視覺解釋
- 在數字放射學中,實施劑量監測對於劑量最佳化至關重要。先前為膠片/螢幕放射學制定的工作人員指南應包括適當的準直、源到影像距離 (SID)、焦點尺寸和患者體位。這些資訊還可以使人們能夠隨後估算有效劑量,例如在沒有 DAP 計的情況下。使用不同檢查的影像質量指標是幫助臨床管理劑量和影像質量之間平衡的另一個步驟[37]。
- 圖 4.17 總結了 1980 年至 2007 年間劑量調查綜合目錄的結果。可以看出,普通放射攝影的有效劑量變化幅度大於 1000 倍,範圍為 0.001 至 3 mSv,具體取決於照射的解剖部位。用於鋇餐檢查的放射攝影/透視程式可以看出會產生更高的劑量 (4-8 mSv),CT 檢查也是如此 (2-16 mSv)。介入放射學被認為會產生更高的劑量 (5-70 mSv)。因此,CT 和介入暴露可以被認為是相對高劑量的檢查,因此需要從劑量管理的角度給予更多關注。但是,應該認識到這些值存在很大的不確定性,其變化幅度可能在 5-10 倍或更多。此外,平均數字本身是按年齡和性別平均的,在應用於個體患者時也會有 ±40% 的變化,具體取決於患者的體重、姿勢、X 射線曝光因素和使用的成像技術等變數。因此,很明顯,它們應該被視為指示性值,不應代替特定檢查對個體患者的劑量。在這裡使用它們僅僅是為了提供劑量管理的比較依據。
- 最後一點,請注意,普通放射攝影、透視檢查、乳腺X線攝影和計算機斷層掃描的患者劑量在 Huda 等人的文章中進行了回顧 (2008)[38]。
參考文獻
[edit | edit source]- ↑ Neitzel U, 2005. CR 和 DR 數字探測器技術的現狀和前景. Radiat Prot Dosimetry, 114:32-8.
- ↑ Cowen AR, Davies AG & Kengyelics SM, 2007. 計算機放射攝影系統及其物理成像特性的進展. Clin Radiol, 62:1132-41.
- ↑ Schaefer-Prokop CM, De Boo DW, Uffmann M & Prokop M, 2009. DR 和 CR:技術的最新進展. Eur J Radiol, 72:194-201.
- ↑ Cesar LJ, Schueler BA, Zink FE, Daly TR, Taubel JP & Jorgenson LL, 2001. 計算機放射攝影中發現的偽影. Br J Radiol, 74:195-202.
- ↑ Cowen AR, Davies AG & Sivananthan MU, 2008. 用於數字透視檢查和透視攝影的動態、固態、平板X射線影像探測器的設計和成像特性. Clin Radiol, 63:1073-85.
- ↑ Cowen AR, Kengyelics SM & Davies AG, 2008. 固態、平板、數字放射攝影探測器及其物理成像特性. Clin Radiol, 63:487-98.
- ↑ Spahn M, 2005. 平板探測器及其臨床應用. Eur Radiol, 15:1934-47.
- ↑ Sato K, Nariyuki F, Kuwabara T, Fukui S, Okada Y, Nabeta T, Hosoi Y, Enomoto J, Sasao M & Seguchi Y, 2010. CALNEO 的開發,一種具有高轉換效率的間接轉換數字放射攝影系統. Fujifilm R&D, 55:10-3
- ↑ Rivetti S, Lanconelli N, Bertolini M, Borasi G, Golinelli P, Acchiappati D & Gallo E, 2009. 用於數字乳腺X線攝影的新型臨床系統的物理和心理物理表徵. Med Phys, 36:5139-48
- ↑ Balter S, 2019. 從 1895 年到 2019 年的透視技術驅動因素:物理學和生理學. Medical Physics International, 7:111-40.
- ↑ Seibert JA, 2006. 平板探測器:它們到底好在哪裡?. Pediatr Radiol, 36 Suppl 2:173-81.
- ↑ Yaffe MJ & Rowlands JA, 1997. 用於數字放射攝影的 X 射線探測器. Phys Med Biol, 42:1-39.
- ↑ Schuncke A & Neitzel U, 2005. 對數字放射攝影系統在常規臨床使用中的回顧性患者劑量分析. Radiat Prot Dosimetry, 114:131-4.
- ↑ Prieto C, Vano E, Ten JI, Fernandez JM, Iñiguez AI, Arevalo N, Litcheva A, Crespo E, Floriano A & Martinez D, 2009. 使用 DICOM 頭部資訊對數字放射攝影中的影像重拍進行分析. J Digit Imaging, 22:393-9.
- ↑ Shope TS, 1996. 透視檢查引起的放射性皮膚損傷. Radiographics, 16:1195-9.
- ↑ Valentin J, 2000. 避免醫療介入程式中出現的放射性損傷. Ann ICRP, 30:7-67.
- ↑ Balter S, Hopewell JW, Miller DL, Wagner LK & Zelefsky MJ, 2010. 透視引導介入程式:患者皮膚和毛髮放射性影響的回顧. Radiology, 254:326-41.
- ↑ Lin PJ, 2007. 透視系統自動劑量控制與光譜整形濾波器結合的操作邏輯. Med Phys, 34:3169-72.
- ↑ Vañó E, González L, Beneytez F & Moreno F, 1998. 非最佳化介入放射實驗室中職業暴露引起的晶狀體損傷. Br J Radiol, 71:728-33.
- ↑ Tremains MR, Georgiadis GM & Dennis MJ, 2001. 使用反C臂技術在四肢手術中的輻射暴露. J Bone Joint Surg Am, 83-A:674-8.
- ↑ Whitby M & Martin CJ, 2003. 執行介入程式的放射科醫師腿部的輻射劑量:它們會導致問題嗎?. Br J Radiol, 76:321-7.
- ↑ Shortt CP, Al-Hashimi H, Malone L & Lee MJ, 2007. 介入放射學中工作人員下肢的輻射劑量. Cardiovasc Intervent Radiol, 30:1206-9.
- ↑ Shortt CP, Fanning NF, Malone L, Thornton J, Brennan P & Lee MJ, 2007. 神經介入手術中的甲狀腺劑量:鉛遮蔽能降低劑量嗎?. Cardiovasc Intervent Radiol, 30:922-7.
- ↑ Thornton RH, Dauer LT, Altamirano JP, Alvarado KJ, St Germain J & Solomon SB, 2010. 比較介入放射室中操作人員眼睛保護策略. J Vasc Interv Radiol, 21:1703-7.
- ↑ Vano E, Kleiman NJ, Duran A, Rehani MM, Echeverri D & Cabrera M, 2010. 介入心臟病學人員的輻射性白內障風險. Radiat Res, 174:490-5.
- ↑ Jacob S, Michel M, Spaulding C, Boveda S, Bar O, Brézin AP, Streho M, Maccia C, Scanff P, Laurier D & Bernier MO, 2010. 介入心臟病學中的職業性白內障和晶狀體混濁(O'CLOC 研究):X 射線是否參與?輻射性白內障和晶狀體混濁. BMC Public Health, 10:537.
- ↑ Martin CJ, 2009. 放射工作人員劑量和劑量監測要求的回顧. Radiat Prot Dosimetry, 136:140-57.
- ↑ Hellawell GO, Mutch SJ, Thevendran G, Wells E & Morgan RJ, 2005. 輻射暴露和泌尿科醫師:風險是什麼?. J Urol, 174:948-52.
- ↑ Walsh SR, Cousins C, Tang TY, Gaunt ME & Boyle JR, 2010. 血管內介入中的電離輻射. J Endovasc Ther, 15:680-7.
- ↑ Le Heron J, Padovani R, Smith I & Czarwinski R, 2010. 醫療工作人員的輻射防護. Eur J Radiol. 2010 Oct;76(1):20-3.
- ↑ Wallace AB, Goergen SK, Schick D, Soblusky T & Jolley D, 2010. 多層螺旋CT 劑量:來自成功最佳化計劃的臨床實踐改進策略. J Am Coll Radiol, 7:614-24.
- ↑ Ruiz-Cruces R, Perez-Martinez M, Martin-Palanca, Flores A, Cristófol J, Martínez-Morillo M & Díez de los Ríos A, 1997. 放射引導介入血管手術中的患者劑量:傳統系統與數字系統. Radiology, 205:385-93.
- ↑ Ruiz-Cruces R, Ruiz F, Pérez-Martínez M, López J, Tort Ausina I 和 de los Ríos AD,2000. 鋇劑檢查的患者劑量. Br J Radiol, 73:752-61.
- ↑ a b Mettler FA Jr, Huda W, Yoshizumi TT 和 Mahesh M,2008. 放射學和診斷核醫學的有效劑量:目錄. 放射學, 248:254-63.
- ↑ Shortt CP, Malone L, Thornton J, Brennan P 和 Lee MJ,2008. 診斷腦血管造影過程中對眼睛和甲狀腺的輻射防護:一項體模研究. J Med Imaging Radiat Oncol, 52:365-9.
- ↑ Davies AG, Cowen AR, Kengyelics SM, Moore J, Pepper C, Cowan C 和 Sivanathan MU,2006. 在熒光透視引導下的心臟電生理檢查中降低 X 射線劑量. Pacing Clin Electrophysiol, 29:262-71.
- ↑ Uffmann M 和 Schaefer-Prokop C,2009. 數字放射學:影像質量與所需輻射劑量之間的平衡. Eur J Radiol, 72:202-8.
- ↑ Huda W, Nickoloff EL 和 Boone JM,2008. 過去 50 年美國診斷放射學患者劑量學概述. Med Phys, 35:5713-28.