有機化學/手性/非對映異構體
非對映異構體是立體異構體,它們不是彼此的對映異構體(映象)。由於它們的形狀不同,非對映異構體可能具有不同的物理和化學性質。對於生物系統中涉及的非對映異構體,這可能尤其如此。
根據 IUPAC,術語“幾何異構”是“順反異構”的過時同義詞,強烈建議不要使用。有時,“幾何異構”一詞已被用作立體異構的同義詞,即光學異構體被認為是幾何異構體。但是,這與當前標準化學命名法不一致。對於不是光學異構體的立體異構體的精確術語是非對映異構體。
非對映異構體的一種特殊型別是差向異構體。差向異構體是在多個不對稱碳原子中僅在一個不對稱碳原子處不同的非對映異構體。還有一種叫做端基異構體的東西,它是一種特殊的差向異構體。端基異構體是在形成環時(在碳水化合物化學中)在一個新的不對稱碳原子處不同的差向異構體。
當存在雙鍵時,可能會發生立體異構,因為涉及的π鍵阻止該鍵以與單鍵相同的方式“扭曲”。一個很好的例子是 1,2-二氯乙烯:C2H2Cl2。考慮以下兩個例子
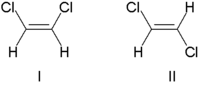
上面顯示的兩個分子是順-1,2-二氯乙烯和反-1,2-二氯乙烯。這兩個分子是幾何異構體,因為由於它們之間π鍵引起的剛性,兩個碳原子不能彼此旋轉。因此,它們不是“可重疊的” - 它們不相同,也不能互相取代。順/反異構體具有不同的化學和物理性質,並且可能表現出截然不同的生物活性。
順反異構(通常稱為幾何異構,儘管此術語是指所有立體異構體)是立體異構的一種形式,它描述了鍵兩端的官能團的取向,該鍵周圍沒有旋轉。烯烴和環烷烴都限制了某些鍵周圍的旋轉。在烯烴中,雙鍵限制了運動和旋轉,環烷烴的環狀結構也是如此。
烯烴雙鍵周圍可以旋轉,但這需要 60 到 70 千卡的能量。如果不新增這種能量,從雙鍵一側開始的基團就會停留在那裡。這就是順/反異構的基礎。
有兩種形式;順式和反式異構體。取代氫原子位於不允許旋轉的鍵的同一側的形式稱為順式;取代氫原子位於鍵的相對側的形式稱為反式。顯示順反異構的小烴的一個例子是 2-丁烯。
物質的順式異構體和反式異構體具有不同的物理性質。反式異構體通常具有更高的沸點和更低的密度。這是因為反式異構體分子比順式異構體分子更容易排列和相互配合。兩種具有截然不同性質的異構體是馬來酸和富馬酸。這些名稱是 2-丁烯二酸的兩個普通名稱,分別是順式和反式異構體。
環烷烴和類似的化合物也可以表現出順反異構。作為由於環狀結構而導致的幾何異構體的例子,請考慮 1,2-二氯環己烷。這些化合物可以使用R/S 命名法更嚴格地命名。

|

|
| 順-1,2-二氯環己烷 | 反-1,2-二氯環己烷 |
| 1(R),2(S)-二氯環己烷 | 1(S),2(S)-二氯環己烷 |
主條目:E-Z 系統
當雙鍵上有兩個以上不同的取代基時,用於命名異構體的反式/順式系統會失效。(順/反系統只能在所涉及的碳原子都連線有氫原子的情況下使用)。E/Z 命名法是不含糊的。Z(來自德語zusammen)意為“一起”,通常對應於術語順式;E(來自德語entgegen)意為“相對”,通常對應於術語反式。
通常,E 異構體比 Z 異構體更穩定,因為存在空間效應。當兩個大的基團彼此更靠近時,就像它們在 Z 中經常出現的那樣,它們彼此干擾更多,並且比在 E 中具有更高的勢能,在 E 中,大的基團距離更遠,彼此干擾更少。
簡單來說,如果只有一個手性中心在兩個立體異構體之間不同,則兩個立體異構體是彼此的非對映異構體。也就是說,如果兩個分子都包含兩個或多個手性中心,但如果每個分子中只有一個手性中心不同於另一個,則這兩個分子是彼此的非對映異構體。
如果一個分子包含一個不對稱碳原子或立體中心,它將具有兩種映象形式。如果一個分子包含兩個不對稱碳原子,則有四種可能的構型,從數學和物理上來說,所有四種構型都無法彼此為映象。分子中手性中心越多,不同構象異構體的可能性就越多,因此可能存在的非對映異構體就越多。
例如,酒石酸包含兩個不對稱中心,但酒石酸分子的兩種構型彼此等效 - 它們統稱為內消旋化合物。這種構型沒有光學活性,而其餘兩種構型是D- 和L- 映象。因此,酒石酸的內消旋形式是其他形式的非對映異構體。

|

| |
|
(天然)酒石酸 |
D-(-)-酒石酸 |
內消旋酒石酸 |
|
(1:1) |
||
用於區分非對映異構體的兩個常用字首是蘇式和赤式。當以費歇爾投影式繪製時,赤式異構體在同一側具有兩個相同的取代基,而蘇式異構體在相對側具有兩個相同的取代基。
5 碳和 6 碳碳水化合物家族包含許多非對映異構體,因為這些分子中存在大量不對稱中心。由於醛糖(一種型別的碳水化合物)的主鏈中的每個碳以及酮糖(另一種型別的碳水化合物)的主鏈中除一個碳以外的所有碳都連線有氫和羥基,因此任何給定糖中的大多數碳實際上都是手性的。由於手性分子的可能構象數量是 2 的n 次方(2n),其中n 是手性中心的個數,這使得碳水化合物具有很大的變異性,並且存在大量的非對映異構體。

|

|

|
|
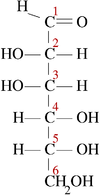
| D-葡萄糖 | L-葡萄糖 | D-半乳糖 | D-甘露糖 |
葡萄糖在溶液中採用環狀結構。這對於費歇爾投影式來說非常尷尬,因此通常使用霍沃思投影式來代替
費歇爾投影式右側的 -OH 基團在霍沃思投影式中繪製在環下方。
非對映選擇性是指在一個有機反應中,一種或多種非對映異構體比另一種更優先形成。





