結構生物化學/放能反應
外觀
< 結構生物化學
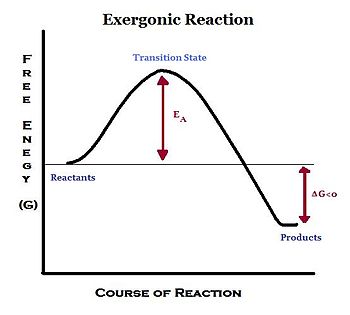
放能反應是指一個釋放能量的反應。由於反應物失去能量(G 減少),在恆溫恆壓下吉布斯自由能(ΔG)為負。這些反應通常不需要能量來進行,因此自發發生。在化學反應中,原子之間鍵的斷裂和形成是一種能量形式。由於化學反應主要由化學鍵的形成和/或斷裂組成,放能反應透過斷裂較不穩定的化學鍵和形成更穩定的鍵來釋放能量。發生在我們身體中的放能反應的例子是細胞呼吸:C6H12O6(葡萄糖) + 6 O2 -> 6 CO2 + 6 H2O 此反應釋放能量,用於細胞活動。
然而,一些放能反應並不自發發生,需要少量的能量輸入來啟動反應。這種能量輸入稱為活化能。一旦活化能需求由外部來源滿足,反應便開始斷裂鍵並形成新鍵,並且在反應進行時釋放能量。這導致周圍系統能量淨增,以及反應系統能量淨減;因此,吉布斯自由能 (ΔG) 的變化為負 (ΔG < 0)。負 ΔG 表明反應是自發的並且熱力學上有利的。
以下是一個 ATP 提供能量的吸能反應。首先,分解 ATP 形成 ADP 和 Pi 是一個放能反應,其中 Delta G 小於 0。然而,透過將反應葡萄糖+Pi ---> 葡萄糖 6-磷酸結合起來,這是一個熱力學上不利的反應。細胞可以驅動吸能反應。
放能反應是
- 最終狀態的自由能 < 初始狀態的自由能
- 反應過程中自由能是自由的
- 能量可以用於進行生物學工作
- 能夠在自發反應中發揮作用
- 不必以很高的速率發生,這就是酶的作用所在
- -ΔG(負數)
http://academic.brooklyn.cuny.edu/biology/bio4fv/page/exergon.htm
