結構生物化學/個性化醫療


儘管在過去幾十年中,透過結構生物化學取得了許多藥理學進展,但所開具的藥物對服用這些藥物的患者中不到一半有效。原因是,雖然大多數人相似,但每個人的基因組都略有不同,對相同藥物的反應也不同。根本原因是,在產生細胞色素P450的基因中存在變異。細胞色素P450(右圖所示)是指一個龐大而多樣化的酶家族,它們處理我們服用的藥物。因此,我們對藥物的反應與基因變異的數量一樣多。
然而,如果瞭解患者的整個基因組,預測哪些藥物有效以及哪些藥物效果最差將相對容易。這就是個性化醫療背後的理念,它是一種醫療模式,利用來自患者基因組和蛋白質組的資訊來最佳化其醫療保健。個性化醫療是藥物階梯模型(右圖所示)的最終目標。最低階是使用重磅藥物;更高階的是分層藥物水平;最高階是個性化醫療,是三種技術中最精確和最準確的患者護理技術。
在過去的五十年裡,主要的醫療模式一直是“重磅藥物”,即對大多數普通人群有效的藥物。具體來說,重磅藥物是指每年為專利權人創造超過10億美元收入的藥物。一些過去的重磅藥物的例子包括立普妥、塞來昔布和耐信。生物化學領域的領先科學家承認,我們正在慢慢地離開重磅藥物時代,並正在向第二階段,分層藥物邁進。
分層藥物是指管理具有共同生物學特徵(例如基因突變的存在與否)的患者群體。分子診斷測試用於確認這些相似性;然後,選擇最最佳化的治療方法,以期為該群體取得最佳結果。分層藥物在實踐中的一個例子是將患有乳腺癌且雌激素受體陽性或HER2過度表達的患者進行分組,並根據這些特徵用抗雌激素或HER2抑制劑進行治療。
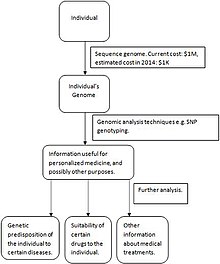
最後,個性化醫療是我們尚未完全實現的期望目標。需要進行蛋白質組學分析、代謝組學分析和每個人的基因檢測,以最佳化預防性和治療性護理。右側的圖表總結了個性化醫療成功所需的關鍵步驟。首先,對個人的基因組進行測序。隨著技術測序技術的發展,基因組測序的成本將下降,使個性化醫療模式更易獲得,也更經濟。然後,使用基因組分析技術,如SNP基因分型和微陣列,以收集有關哪些藥物最有效的資訊(例如,關於個人對某些疾病的遺傳易感性以及特定藥物有效的時間)。個性化醫療取得進展的當前例子是對乳腺癌、肺癌和結直腸癌患者的erbB2和EGFR蛋白的測量,並在選擇適當的治療方法之前進行。隨著個性化醫療領域的進步,從組織中闡明的分子資訊將與患者的醫療和家族史、影像學資料以及大量的實驗室檢測結果相結合,為更廣泛的疾病開發更有效的治療方法。
由於每個人都有獨特的基因組,透過藥理基因學方法實現個性化醫療的優勢包括
1. 提高藥物的有效性 例如,使用正確的藥物和劑量,使藥物更容易被患者的身體吸收
2. 減少副作用
PricewaterhouseCoopers' Health Research Institute,(2009)。[個性化醫療的新科學] http://www.pwc.com/personalizedmedicine
Shastry BS (2006)。“藥理基因學與個體化醫療的概念”。《藥理基因組學雜誌》。6(1):16–21。
2010-2014 年醫藥市場趨勢,來自 Urch Publishing
Jørgensen JT,Winther H. 個性化醫療的新時代:10 年後。《個性化醫療》2009;6:423-428。
