結構生物化學/類維生素 A
類維生素 A 和類胡蘿蔔素是其化學和代謝與特定加工蛋白協同作用,幫助解釋視覺的化學基礎的分子。由於類維生素 A 和類胡蘿蔔素都被歸類為異戊二烯,它們在化學轉化方面有限。有趣的是,由於這些基因被發現在昆蟲和脊椎動物視覺的形成中高度保守,並且參與生色團的產生和迴圈,因此人們提出了關於視覺化學共同祖先起源的概念,並得到了發展。

視覺生色團的順式到反式異構化迴圈是動物視覺的內在機制。
G 蛋白訊號傳導是一種訊號轉導途徑,其中七次跨膜受體,如視紫紅質,響應各種化學訊號(激素、神經遞質等),啟用異三聚體 G 蛋白,並幫助執行一系列事件,這些事件負責整個身體的許多生理過程。
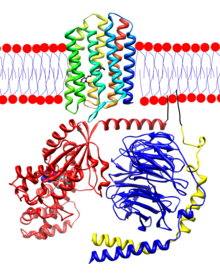
人們發現,視覺色素構成了一類 G 蛋白偶聯受體,並具有視蛋白(完整的跨膜蛋白)和一個共價連線的視黃醛生色團等組分,該生色團參與光轉導過程。
視覺 GPCR 訊號傳導需要一種飲食來源的生色團,該生色團是透過類胡蘿蔔素(C40)氧化裂解成類維生素 A(C20)自然產生的。然後,類維生素 A 被轉化為 11-順式視黃醛衍生物(脊椎動物為 2-脫氫視黃醛,昆蟲為 3-羥基視黃醛)。然後,這些視黃醛衍生物會與視蛋白中 Lys 殘基形成席夫鹼鍵,以建立功能性視覺色素。當光被吸收時,所有順式生色團將異構化為反式異構體,隨後將視紫紅質轉化為稱為 Meta II 的啟用狀態。Meta II 結合轉導蛋白(感光器特異性 G 蛋白),啟動導致質膜超極化的級聯反應。

為了再生順式生色團,人們研究了一種稱為類維生素 A 迴圈的酶促途徑。該迴圈涉及桿狀感光細胞和錐狀感光細胞。桿狀感光細胞消耗順式異構體,儘管在強光下被錐狀感光細胞飽和。因此,人們提出了一種錐狀感光細胞特異性再生途徑,以避免這兩種受體之間的競爭。如果發生在編碼重要組分(例如促進生色團飲食前體(類胡蘿蔔素和類維生素 A)的吸收、運輸、代謝和儲存途徑的蛋白質)的基因中發生突變,可能會導致失明疾病和更致命的疾病,如馬修-伍德綜合徵。
迴圈過程的第一步由視黃醇脫氫酶 (RDHs) 完成,其中所有反式視黃醛都被還原為反式視黃醇。主要的 RDH 是外節 (OS) 感光細胞中的 RDH8 和感光細胞內節中的 RDH12(還有其他 RDH)。所有反式視黃醇都被從 OS 運輸到 RPE,在那裡它們被酯化。這一過程由兩種類維生素 A 結合蛋白促進,稱為感光間視黃醇結合蛋白 (IRBP) 和細胞視黃醇結合蛋白 1 (CRBP1)。這些反式視黃醇酯形成維生素 A 和稱為視黃醇體的油滴結構的穩定儲存形式。然後,酶 RPE65 催化將所有反式類維生素 A 轉化為 11-順式視黃醇的吸熱反應。在最後一步,RDH5、RDH10 和 RDH11 等酶催化將 11-順式視黃醇氧化為維持視覺所需的原始 11-順式視黃醛。然後,這些 11-順式視黃醛與細胞視黃醛結合蛋白 (CRALBP) 結合,CRALBP 介導其運輸回感光細胞 OS 和視蛋白。
在錐狀感光細胞再生途徑中,從錐狀感光細胞 OS 釋放的所有反式視黃醇都被運輸到穆勒細胞而不是 RPE。在那裡,它們被異構化為 11-順式異構體形式,並透過醯基輔酶 A:視黃醇醯基轉移酶 (ARAT) 酯化為 11-順式視黃醇酯。這些酯在 11-順式視黃醇酯水解酶 (REH) 的幫助下轉化為 11-順式視黃醇,然後它們與 CRALBP 結合並被帶回錐狀感光細胞受體。在最後一步,NADP+/NADPH 依賴性 11-順式 RDH 活性促進了視覺生色團的再生。
視覺迴圈酶是一系列微粒體酶,它們促進反式視黃醇向順式視黃醛的轉化。它們通常是膜結合酶,這使得它們難以研究,因為在 X 射線晶體學進行之前需要使用去垢劑。類胡蘿蔔素氧化酶 (ACO) 是一種 RPE65 酶的水溶性同源物,屬於類胡蘿蔔素裂解氧化酶 (CCO) 家族。ACO 的結構表明 CCO 含有 7 葉 β-螺旋槳通用摺疊,並且亞鐵離子輔因子透過四個高度保守的 His 殘基配位。來自牛的天然 RPE65 的結構表明,將蛋白質插入活性位點只有一種方式。這是透過在 RPE65 中發現的單個通道來識別的,該通道允許底物的進入和產物的釋放。根據這種結構推斷,科學家們提出類維生素 A 底物從膜中進入活性位點,產物從活性位點進入膜中的另一個組分 (RDH5) 進行進一步加工。這些過程恰好在內質網膜中發生,不涉及類維生素 A 結合蛋白。
有四種主要的視黃醇/視黃醛結合蛋白;它們是 RBP、CRBP、IRBP 和 CRALBP。RBP 和 CRBP 是具有單個結構域的杯形蛋白。配體結合的活性位點由疏水性反平行 β-桶摺疊組成,這些摺疊只對反式視黃醇分子具有親和力。結合的視黃醇在 RBP 和 CRBP 中的取向不同。當在 RBP 中發現時,它們往往會聚集在空腔入口周圍。相反,它們在 CRBP 中的空腔底部被發現。
IRBP 是一種由感光細胞神經元產生的可溶性脂蛋白。它的主要功能被認為是促進類維生素 A 在感光細胞和 RPE 的細胞層之間的運輸。與 RBP 和 CRBP 中觀察到的單個結構域相反,該蛋白質包含大約三到四個類維生素 A 結合位點。該蛋白質採用桿狀結構,並且在配體結合時,構象發生改變為彎曲的分子結構。在進一步的結構分析中,揭示了兩個疏水性空腔是潛在的配體結合位點。

CRALBP 屬於一個蛋白質家族,這些蛋白質在自然狀態下結合疏水配體,並且由一簇高度鹼性氨基酸殘基組成。高解析度結構分析表明,11-順式視黃醛深深地結合在蛋白質空腔中,配體中心最靠近空腔入口。與在視紫紅質中其順式雙鍵發生扭曲(在光觸發時轉化為反式)相反,視黃醛分子在與 CRALBP 結合時採用完美的順式構型。這使得順式到反式異構化極不穩定。因此,視黃醛可以在運輸到視蛋白和感光細胞 OS 時保持其順式構型。
類維生素 A 中的共軛雙鍵在光觸發時進行異構化。在光感知下,11-順式視黃醛被轉化為全反式視黃醛。在該反應機制中,雙鍵透過光子提供的能量暫時斷裂。為了再生光敏生色團,需要一個稱為異構水解酶(也稱為類維生素 A 異構酶)活性的過程。該酶催化水與碳正離子的反應。在光化學途徑的情況下,該酶催化再生順式構型視黃醛的過程。然而,從理論化學機制的角度來看,水對該分子的異構化和水解似乎並不可行。雖然已經提出了許多反應機制,但 Sn1 親核取代似乎是最合理的機制。在該反應中,在酯基透過三價鐵/二價鐵離子輔因子和 RPE65 的烷基裂解後,會生成一個非常穩定的雙鍵共軛碳正離子。親核試劑的加入完成了將全反式視黃醇酯轉化為 11-順式視黃醇的轉化。
1. Von Lintig J, Kiser PD, Golczak M, Palczewski K. "類維生素 A 在視覺化學中的反式到順式異構化的生化和結構基礎。" Trends Biochem Sci. 2010 Jul;35(7):400-10. Epub 2010 Feb 24.
2. 維基百科貢獻者。"轉導蛋白。" 維基百科,自由的百科全書。維基百科,自由的百科全書,2012 年 11 月 7 日。網路。2012 年 12 月 6 日。
3. 維基百科貢獻者。 “生色團”。 維基百科,自由的百科全書。 維基百科,自由的百科全書,2012年8月26日。 網頁。 2012年12月6日。
4. 維基百科貢獻者。 “視黃醇結合蛋白”。 維基百科,自由的百科全書。 維基百科,自由的百科全書,2012年7月7日。 網頁。 2012年12月7日。
