核醫學基礎物理/核醫學成像系統

我們在這本華夏公益教科書中涵蓋的主題包括放射性,伽馬射線與物質的相互作用以及輻射探測。遵循這條途徑的主要原因是將我們帶到本章的主題:核醫學成像系統。這些是產生放射性物質在給藥後在患者體內分佈圖像的裝置。
放射性通常以 放射性藥物 的形式給患者服用 - 術語 示蹤劑 也被使用。它遵循某些生理途徑在身體的某個部位積累一段時間。一個很好的例子是 99mTc-錫膠體,在靜脈注射後主要積聚在患者的肝臟中。該物質在患者肝臟中時會發出伽馬射線,我們可以使用核醫學成像系統生成其分佈圖像。這張影像可以告訴我們肝臟的功能是否正常或異常,或者它的一部分是否因某種疾病而受損。
不同的放射性藥物用於生成幾乎所有身體部位的影像
| 身體部位 | 示例示蹤劑 |
|---|---|
| 大腦 | 99mTc-HMPAO |
| 甲狀腺 | Na99mTcO4 |
| 肺(通氣) | 133Xe 氣體 |
| 肺(灌注) | 99mTc-MAA |
| 肝臟 | 99mTc-錫(或硫)膠體 |
| 脾臟 | 99mTc-受損紅細胞 |
| 胰腺 | 75Se-硒代蛋氨酸 |
| 腎臟 | 99mTc-DMSA |
請注意,使用這種成像方法獲得的資訊形式主要與器官的生理功能有關,而不是主要使用 X 射線成像系統獲得的解剖資訊。因此,核醫學提供了對疾病狀況的不同視角,並生成 X 射線影像以外獲得的附加資訊。我們這裡的目的是集中在用於生成影像的成像系統上。
該領域早期使用的成像系統包括輻射探測器(例如閃爍探測器),該探測器緩慢地掃描患者的某個區域,以測量該區域內各個點的輻射強度。其中一種裝置被稱為 直線掃描器。自 1970 年代以來,此類成像系統已被更復雜的裝置取代,這些裝置可以更快地生成影像。這些現代裝置中最常見的一種稱為 伽馬相機,我們將在下面考慮其結構和工作方式。Slomka 等人在 (2009)[1] 中對該技術在心臟應用方面的最新進展進行了回顧。
當今使用最廣泛的伽馬相機型別的基本設計是由一位美國物理學家 哈爾·安格 開發的,因此有時被稱為安格相機。它包含一個直徑較大的 NaI(Tl) 閃爍晶體,該晶體由大量光電倍增管觀察。
下圖顯示了伽馬相機基本元件的框圖

晶體和光電倍增管被安裝在一個通常稱為 相機頭 的圓柱形外殼中,該圖顯示了它的橫截面檢視。晶體可以是大約 25 釐米到 40 釐米的直徑,大約 1 釐米厚。直徑取決於裝置的應用。例如,用於心臟應用的相機可能會使用 25 釐米直徑的晶體,而用於生成肺部影像的相機可能會使用 40 釐米的較大晶體。晶體的厚度是經過選擇的,以便它對 99mTc 發出的 140 keV 伽馬射線提供良好的檢測 - 它是當今使用最廣泛的放射性同位素。
在晶體中產生的閃爍被大量光電倍增管檢測到,這些光電倍增管以二維陣列排列。現代伽馬相機中通常有 37 到 91 個光電倍增管。這些光電倍增管產生的輸出電壓被饋送到一個位置電路,該電路產生四個輸出訊號,稱為 ±X 和 ±Y。這些位置訊號包含有關閃爍在晶體內產生位置的資訊。在最基本的伽馬相機設計中,它們被饋送到 陰極射線示波器 (CRO)。我們將在下面詳細描述 CRO 的工作原理。
在我們這樣做的之前,我們應該注意到位置訊號還包含有關每個閃爍強度的資訊。可以透過將位置訊號饋送到一個求和電路(圖中標記為 ∑)來推匯出這種強度資訊,該電路將四個位置訊號相加以生成一個電壓脈衝,該脈衝表示閃爍的強度。這個電壓脈衝通常被稱為 Z 脈衝,在經過脈衝高度分析 (PHA) 後,它被作為 非遮蔽脈衝 饋送到 CRO。
因此,我們最終得到四個位置訊號和一個非遮蔽脈衝傳送到 CRO。讓我們簡要回顧一下 CRO 的工作原理,然後繼續。CRO 的核心包含一個真空管,一端是電子槍,另一端是塗有熒光粉的螢幕。電子槍產生電子束,該電子束被引導到螢幕,螢幕在電子束撞擊的點發射光。電子束的位置可以透過垂直和水平偏轉板控制,並透過將適當的電壓饋送到這些板,電子束可以定位在螢幕上的任何點。示波器的正常工作模式是使電子束保持開啟狀態。在伽馬相機的情況下,CRO 的電子束通常處於關閉狀態 - 它被稱為 遮蔽。
當 PHA 電路產生非遮蔽脈衝時,CRO 的電子束會短暫開啟,以便在螢幕上顯示一道閃光。換句話說,來自 PHA 電路的電壓脈衝用於非遮蔽 CRO 的電子束。
那麼,這道閃光出現在 CRO 螢幕上的什麼位置呢?閃光的位置由位置電路產生的 ±X 和 ±Y 訊號決定。正如你可能猜到的那樣,這些訊號被饋送到 CRO 的偏轉電路,以便使非遮蔽電子束撞擊螢幕上的一個與閃爍在 NaI(Tl) 晶體內最初產生位置相關的點。很簡單!
因此,伽馬相機可以被認為是一種複雜的電子電路排列,用於將閃爍晶體中閃光的位置轉換為示波器螢幕上相關點的閃光。此外,在電路中使用脈衝高度分析儀使我們能夠透過拒絕所有電壓脈衝(除了發生在伽馬射線能量譜的光峰內的電壓脈衝)來轉換僅與晶體中光電事件相關的閃爍。
在我們繼續之前,讓我們 總結 我們已經做到了什麼。放射性藥物被給予患者,它積聚在目標器官中。伽馬射線從器官向各個方向發射,那些朝著伽馬相機方向的射線進入晶體併產生閃爍(請注意,在晶體前面有一個名為 準直器 的裝置,我們將在後面討論)。閃爍被一系列光電倍增管檢測到,這些光電倍增管的輸出被饋送到一個位置電路,該電路生成四個與閃爍在晶體內的位置相關的電壓脈衝。這些電壓脈衝被饋送到 CRO 的偏轉電路。它們也被饋送到一個求和電路,該電路的輸出(Z 脈衝)被饋送到 PHA,而 PHA 的輸出用於開啟(即,非遮蔽)CRO 的電子束。一道閃光出現在 CRO 螢幕上的一個與閃爍在 NaI(Tl) 晶體內發生位置相關的點。因此,當從器官發射的伽馬射線被晶體檢測到時,在 CRO 螢幕上形成器官內放射性藥物分佈的影像。
我們在上面描述的是相當傳統的伽馬相機的操作。現代設計要複雜得多,但基本設計與所描述的幾乎相同。一個設計改進的主要領域是影像形成和顯示領域。最基本的方法是拍攝 CRO 螢幕一段時間,以允許光閃光的積分,從而在 照相膠片 上形成影像。更高一級的做法是使用 儲存示波器,它允許每個閃光在螢幕上保留一段時間。
最現代的方法是將位置和能量訊號饋送到計算機的記憶體電路中進行儲存。因此,記憶體內容可以在計算機顯示器上顯示,也可以以多種方式進行操作(即 處理)。例如,可以使用不同的顏色來表示器官內放射性藥物的不同濃度。
現在,數字影像處理 在核醫學中得到了廣泛應用,因為它可以快速方便地控制影像採集和顯示,以及分析影像或影像序列,用患者姓名和檢查詳細資訊對影像進行標註,儲存影像以便日後檢索,以及透過 網路 將影像資料傳送到其他計算機。
下一張圖展示了現代伽馬相機的重要組成部分。患者發射的伽馬射線穿過準直器,並在相機頭部被探測到,相機頭部會生成與晶體中閃爍位置以及伽馬射線能量相關的資料。然後,電子硬體會對資料進行即時處理,校正空間線性、光電倍增管漂移和能量響應等技術因素,從而產生具有空間均勻靈敏度和無失真效能的成像系統。
多通道分析器(MCA)用於顯示與晶體內相互作用的伽馬射線的能譜。由於這些伽馬射線起源於患者體內,因此其中一些伽馬射線在穿過患者組織(以及其他元件,如患者床和成像系統結構)時會被散射,因此能量會低於光峰。一些散射事件可能只涉及與自由電子的擦邊碰撞,因此伽馬射線只損失少量能量。這些伽馬射線的能量可能略低於光峰,因此它們的譜線與光峰合併。因此,用於成像患者的伽馬相機的光峰包含來自空間相關的、未衰減的伽馬射線(這是我們想要的資訊)以及來自空間不相關的、散射的伽馬射線的。散射的伽馬射線充當真實光峰資料中的可變背景,其效果是伽馬相機影像中的背景霧氣。

雖然散射在平面閃爍成像中可能不是一個重大問題,但它對從伽馬相機影像中獲得的定量資訊的保真度有很大影響,並且是發射斷層掃描準確影像重建的一個重要考慮因素。未衰減的伽馬射線(也稱為**初級**輻射)包含所需的資訊,因為它們與放射性直接相關。
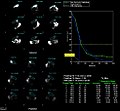
下圖更詳細地說明了散射情況,該圖顯示了在患者成像條件下99mTc的初級和散射譜的估計值。可以使用蒙特卡羅方法生成此類譜估計。從圖中可以看出,散射輻射的能量形成一個寬頻,類似於之前描述的康普頓散射,該寬頻與探測到的光峰合併並對光峰有很大貢獻。因此,探測到的光峰是初級輻射的過高估計。這種過高估計的程度可能取決於具體的成像情況,因為涉及的組織厚度不同。然而,很明顯,如果需要準確測量放射性,則需要考慮探測到的光峰內的散射貢獻。

下圖說明了一種補償散射貢獻的方法,該方法涉及使用來自較低能量視窗的資料作為對光峰進行減去的估計值,即
其中 k 是一個比例因子,用於考慮散射貢獻的程度。這種散射補償方法稱為**雙能量視窗**(DEW)方法。在實踐中,可以透過獲取兩幅影像(每個能量視窗一幅)並從光峰影像中減去散射影像的一部分(k)來實現它。
對於上面顯示的譜線,可以看出比例因子 k 大約為 0.5,但應瞭解,它的確切值取決於散射條件。因此,使用 DEW 方法的伽馬相機通常提供調整 k 以適應不同成像情況的功能。一些系統使用比圖中所示更窄的散射視窗,例如 114-126 keV,從而導致 k 增加到大約 1.0,例如。
還開發了許多其他散射補償方法。這些方法包括更復雜的能量分析形式,例如**雙光峰**和**三能量視窗**技術,以及基於去卷積和光子衰減模型的方法。Zaidi & Koral (2004)對這些發展進行了很好的綜述。

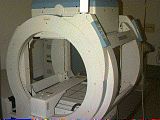
以下展示了一些伽馬相機和相關裝置的照片
 |
 |
 |
 |
 |
 |
 |
 |
我們將繼續描述伽馬相機,並考慮準直器的結構和用途。
準直
[edit | edit source]準直器是一種安裝在伽馬相機頭部前面的裝置。它的作用有點像照相機中使用的鏡頭,但這種類比並不完全正確,因為很難聚焦伽馬射線。然而,在其最簡單的形式中,它用於阻擋所有朝向晶體傳播的伽馬射線,除了那些垂直於晶體平面傳播的伽馬射線。

圖示展示了連線到晶體的**平行孔準直器**的放大檢視。準直器只是在鉛板上鑽了許多小孔。請注意,以一定角度進入晶體的伽馬射線會被鉛吸收,只有沿著孔的方向進入的伽馬射線才能透過,在晶體中產生閃爍。如果沒有準直器,這些斜入射的伽馬射線會使伽馬相機產生的影像模糊。換句話說,影像不會很清晰。
大多數伽馬相機都配有多種準直器,可以根據檢查的需要進行安裝。這些準直器的基本設計相同,但它們在每個孔的直徑、每個孔的深度以及每個孔之間的鉛厚度(通常稱為**隔板厚度**)方面有所不同。特定準直器的選擇取決於發生的輻射吸收量(影響伽馬相機的**靈敏度**),以及它產生的影像的清晰度(即**空間解析度**)。不幸的是,這兩個因素成反比,也就是說,使用產生高空間解析度影像的準直器通常意味著儀器對輻射的靈敏度不是很高。
除了平行孔型別之外,還使用其他準直器設計。例如,**發散**孔準直器產生縮小的影像,**會聚**孔和**針孔**準直器產生放大的影像。針孔準直器在下圖中說明

它通常是一個錐形裝置,其壁由鉛製成。圖中顯示了該圓錐的橫截面。它的工作原理類似於針孔照相機,併產生物體的倒置影像 - 圖中使用箭頭來說明這種反轉。這種型別的準直器被發現對成像小物體(如甲狀腺)很有用。
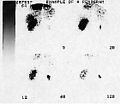
示例影像
[edit | edit source]以下顯示了一些核醫學影像的代表性選擇
發射斷層掃描
[edit | edit source]我們一直在描述的成像形式稱為**平面成像**。它產生三維物體的二維影像。因此,影像不包含深度資訊,一些細節可能會相互疊加,從而被遮擋或部分遮擋。請注意,這也是傳統 X 射線成像的一個特點。
克服這種限制的通常方法是至少對患者進行兩次成像,例如,一次從正面,一次從側面。因此,在胸部 X 光檢查中,可以拍攝前後 (PA) 和側位檢視。在核醫學肝臟掃描中,會採集前後 (AP) 和側位掃描。
平面 X 射線成像的侷限性在 1970 年左右被 CAT 掃描器 的開發所克服。CAT 代表計算機軸向斷層掃描或計算機輔助斷層掃描,如今該術語通常縮寫為計算機斷層掃描或 CT 掃描(斷層掃描一詞源於希臘語 tomos,意思是 **切片**)。無論其確切名稱如何,該技術都允許使用計算機生成穿過人體的切片的影像。它本質上是透過在患者周圍的不同角度拍攝 X 射線影像來實現這一點。這些切片影像顯示了平面圖像中缺失的第三維,從而消除了疊加細節的問題。此外,可以透過使用計算機將穿過患者區域的一系列連續切片的影像堆疊在一起,以生成 三維影像。顯然,與平面成像相比,CT 掃描是一種非常強大的成像技術。
等效的核醫學成像技術稱為 **發射計算機斷層掃描**。我們將在下面考慮該技術的兩種實現方式。
- 下面說明了 反投影 重建過程。為簡單起見,我們假設穿過患者的切片實際上由一個 2x2 體素陣列組成,每個體素的放射性由 A1...A4 給出

- 第一個投影 P1 從右側成像,第二個投影 P2 從右斜側成像,依此類推。反投影過程首先將投影彼此相加,如下所示

- 然後將求和(或疊加)的投影歸一化,以生成對每個體素中放射性的估計。由於此過程會在重建的影像中生成條紋偽影,因此在反投影之前通常會對投影進行濾波,如 後面的章節 中所述,整個過程稱為濾波反投影 (FBP)
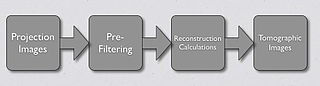
- 另一種影像重建技術稱為 迭代重建,這是一種逐次逼近技術。最大似然期望最大化 (ML-EM) 演算法被廣泛應用,其中使用除法過程來比較實際投影和估計投影,如下所示

- 將資料透過該處理鏈進行一次迴圈稱為一次 **迭代**。可能需要 16 次或更多次迭代才能生成足夠的重建,因此計算時間可能相當長。 有序子集期望最大化 (OS-EM) 演算法可以透過在迭代過程中以順序方式利用有限數量的投影(稱為 **子集**)來顯著減少計算時間。在重建過程中產生的噪聲可以透過使用內置於重建計算中的高斯濾波器或作為後濾波器來減少

- 可以在 線上書籍 中找到使用不同迭代次數、子集和過濾設定生成的影像。
- 下面顯示了這些影像重建技術對穿過患者肺部通氣掃描的切片的比較

- 伽馬相機通常圍繞患者旋轉以採集影像。專門為 SPECT 掃描設計的現代伽馬相機可以由兩個平行安裝的相機頭組成,患者位於兩者之間。因此,生成影像所需的時間減少了大約兩倍。此外,一些專為腦部掃描設計的 SPECT 伽馬相機在三角形排列中安裝了三個相機頭。
- 可以採用各種策略來採集和處理 SPECT 影像。
- 您將從 第二章 中瞭解到正電子可以從放射性核中發射出來,這些核具有過多的中子而導致不穩定。您還將瞭解到正電子在物質中不會存在太久,因為它們很快就會遇到一個電子,併發生一個稱為 **湮滅** 的過程。在這個過程中,正電子和電子消失,它們能量被轉換為兩個以大約 180o 度角彼此發射的伽馬射線。發射通常被稱為兩個 **背靠背** 伽馬射線,它們各自具有 0.51 MeV 的離散能量。
- 因此,如果我們給患者服用一個正電子發射的放射性藥物,發射的正電子會與附近的電子發生湮滅,並且會向相反方向發射兩個伽馬射線。可以使用環繞患者的輻射探測器環來檢測這些伽馬射線,並可以使用計算機系統生成斷層影像。探測器通常是專門的閃爍裝置,它們經過最佳化以檢測 0.51 MeV 的伽馬射線。這種探測器環、相關裝置和計算機系統稱為 PET 掃描器

- 患者體內正電子衰變的位置由上圖中的實心圓突出顯示。此外,出於清晰度的考慮,圖中只顯示了一些探測器。環上的每個探測器與一組相對的探測器一起工作,因此檢測到的湮滅伽馬射線用於建立一個單一的輪廓。
- 人們還發現,配備厚晶體和特殊準直器的伽馬相機可以用於 PET 掃描。
- 用於 PET 掃描的放射性同位素包括 11C、13N、15O 和 18F。這些同位素通常使用一種稱為 迴旋加速器 的儀器來生產。此外,這些同位素的半衰期相對較短。因此,PET 掃描需要一個迴旋加速器和相關的放射性藥物生產設施位於附近。我們將在本華夏公益教科書的 下一章 中討論迴旋加速器。
- 標準攝取值 (**SUV**) 是 PET 中使用的一種半定量指標,用於表示患者掃描中感興趣區域對放射性藥物的攝取。它通常被計算為區域中放射性與注射劑量的比值,並針對體重進行校正。需要注意的是,SUV 受幾個主要變異源的影響,因此不應將其用作定量指標。
- 下面顯示了 PET 掃描器的一些照片
 |
 |
 |
 |
下面顯示了使用迭代重建的不同子集和迭代設定重建的影像[2]

- ↑ Slomka PJ, Patton JA, Berman DS & Germano G, 2009. 心肌灌注 SPECT 成像技術方面的進展. 核心髒病學雜誌,16(2), 255–76.
- ↑ Maher KP, 2016. 迭代次數、子集和高斯過濾,第三版 [Bookemon.com]
- 墨爾本奧斯汀和復原醫療中心的正電子發射斷層掃描中心,包括 PET 簡介、當前設施、專案和研究以及 PET 影像庫