核醫學基礎物理/三維視覺化技術
這是一本名為核醫學基礎物理的華夏公益教科書正在編寫的章節。
三維視覺化技術用於將一系列斷層掃描切片整合到一種形式中,這種形式通常比單獨的切片更容易解釋。本章介紹了醫學成像中使用的主要視覺化技術概述。我們將從二維 (2D) 軸向影像的整合開始,然後再考慮各種三維 (3D) 影像呈現方法。
以下影像集將用於幫助我們完成任務。它們包含一個 SPECT 肺通氣研究(由左側的動畫序列說明)、一個 SPECT 肺灌注研究(在中間)和來自同一患者的 CT 肺血管造影術(CTPA)(在右側)。
 |
 |
 |
我們將在這章的各個階段使用這些影像集,以便提供有助於演示我們將要考慮的技術本質的示例。影像集的採集因素包括 SPECT 研究的每個 128 x 128 畫素切片厚度為 4.8 毫米,CTPA 螺旋掃描重建的軸向影像的每個 512 x 512 畫素連續切片厚度為 1.5 毫米。此外,肺灌注掃描是在通氣掃描之後立即進行的,因此來自前者的殘餘活性以約 20% 的水平存在於後者中。
在繼續之前,考慮一下軸向切片(無論是 SPECT 還是 CT),一個接一個地堆疊在一起,如下圖所示。

請注意,該圖將每個影像表示為一個薄切片,而資料實際上代表一個足夠寬的切片,可以填補它與其下一個切片之間的間隙,因此可以認為影像資料是體積元素矩陣,簡稱體素。
醫學成像中應用的一種慣例是,將軸向影像堆疊顯示為以下圖中所示的軸向。

因此,軸向掃描的左側代表患者的右側,從下方觀看,其前表面位於影像的頂部。斯派克·米利根的一首小曲的改編版可能會幫助你記住這種視角。
| 我多麼想成為一條魚, |
| 能在冰層下游泳, |
| 向上看所有滑冰的人, |
| 哦,那該多好! |
你可能會發現,在閱讀本章時體驗真實情況是一個好主意,這樣有助於克服我們將遇到的許多主題的抽象性,以及使用二維媒介(即本網頁)傳達三維視覺化概念的侷限性。無數開源 3D 程式和影像庫可透過全球資訊網獲取。例如,用於生成本章影像的軟體包括OsiriX(僅適用於 macOS X)、Madena和ImageJ(多平臺)。
我們將要考慮的第一個技術是一個相對簡單的技術,稱為軸向投影。它涉及整合多個軸向影像以顯示一個複合影像,該複合影像呈現該體積影像資料的三維印象。該技術有時被稱為厚板或Z 投影。
下圖說明了一系列 z 投影方法的結果,右下角顯示了一個單切片以供參考。左上角的第一張影像顯示了對 16 個切片求和的結果,同一行上的另外兩張影像分別顯示了計算這些切片的平均值和中位數的結果。

第二行中的前兩張影像分別顯示了最大強度投影(MIP)和最小強度投影(MinIP)的結果。MIP 會評估穿過體積的每條體素線上的每個體素,以確定最大體素值,並使用為每條線確定的這些值形成影像。MinIP 使用最小體素值,如下面的圖所示。

底部一行示例軸向投影集合中的前兩張影像顯示了體繪製投影。這種影像合成方法涉及對體素資料應用不透明度函式以及對所得資料的遞迴新增。以下形式的方程
其中
- An = (α).(體素 n 的體素值),
- Bn = (1-α).(體素 n-1 的體素值),並且
- α = 不透明度,範圍在0(即完全透明)到1(即完全不透明)之間,
應用於每條體素線,如下圖所示。

該圖顯示了我們之前使用過的體素線,右上角有一個不透明度表。顯示的不透明度函式是其中對低於閾值級別的體素值應用零不透明度、對中間範圍的體素值應用不透明度的線性增加、以及對高體素值應用最大不透明度的函式。不透明度表有點像我們之前描述過的用於灰度視窗的查詢表早先,該函式應用於體素值的不透明度而不是它們的灰度級別。請注意,也可以應用比我們在上面的圖中使用的更復雜的不透明度表,例如對數函式和指數函式。
圖的下半部分顯示了計算複合體素的體繪製值的步驟。體素值顯示在第一行,不透明度值顯示在第二行,這些不透明度值來自一個粗略的不透明度表,用於顯示每個體素。第三、第四和第五行詳細說明了A、B和C的值,這些值是使用我們上面的體繪製方程計算得出的。最終的體素值是透過對最後一行求和得到的,並將結果歸一化為,比如說,256 級灰度。
這種處理形式的結果是生成一個影像,該影像包括視覺深度線索,因為類似的體素值將以類似的不透明度顯示,而最靠近參考切片的體素將比來自更遠切片的體素具有更強的貢獻。此外,請注意,每條線中的所有體素值都會對渲染的影像做出貢獻,這與僅對 MIP 或 MinIP 影像做出貢獻的有限數量的體素形成對比。體繪製會產生 3D 效果,如上面的影像所示。
請注意,體繪製可以從遠端到近端切片應用,如我們的圖所示,也可以從相反方向應用,即從近端到遠端切片。因此,我們在上面的一組九個示例影像中使用了體繪製向上和體繪製向下這兩個術語。
選擇適合個體患者研究的軸向投影方法型別取決於診斷過程中相關的解剖和/或功能資訊。例如,讓我們以對我們上面九個示例影像中對比劑填充的血管成像為例。請注意,MIP 可用於直觀地展現患者肺部血管床的印象。但是,這種投影中幾乎沒有深度資訊,因此重疊和底層的血管可能會遮擋目標血管中可能存在的病變。因此,這種軸向投影形式在血管造影中的應用僅限於血管重疊不是問題的研究。在體繪製圖像中包含體素透明度和深度加權解決了 MIP 處理的這一侷限性。
最後需要注意的是,這種影像投影形式也可以應用於軸向切片的多分層重建,我們將在下一節中探討......
多分層重建
[edit | edit source]在最簡單的情況下,多分層重建 (MPR) 涉及生成與軸向切片堆疊成直角的透檢視,以便生成冠狀面和矢狀面影像。我們將從描述這些正交投影開始本節,然後考慮它們同步的複合顯示。我們還將描述該主題的三個變體:斜面重建、曲線重建和整合三維展示。
- 冠狀面重建
- 在這裡,影像堆疊被旋轉,使 z 軸成為垂直軸,並使用平行排列的體素平面重建影像堆疊,這些平面從患者的前表面到後表面排列,如下圖所示

- 以下是我們影像集中示例冠狀面重建的結果
 |
 |
- 在這裡,重建的切片通常從患者的前表面到後表面顯示,患者的頭部朝向切片的頂部,右手側朝向切片的左側。
- 矢狀面重建
- 透過對影像堆疊進行額外的旋轉可以實現矢狀面重建,從而生成患者從左到右的切片序列,如下圖所示

- 以下是我們影像集中示例矢狀面重建的結果
 |
 |
- 在這裡,重建的切片通常從患者的左側顯示到右側,頭部朝向頂部,前表面朝向切片的左側。請注意,也可以使用資料的額外幾何變換生成從右到左的矢狀面堆疊。
- 複合 MPR 顯示
- 冠狀面和矢狀面重建被稱為正交 MPR,因為生成的透檢視來自相互成直角的影像資料平面。可以生成複合 MPR 顯示,以便使用連結的遊標或十字線從所有三個透檢視定位感興趣的點,如下圖所示
 |
 |
- 這種影像展示形式有時被稱為TCS 顯示——意味著檢視Transaxial、Coronal 和 Sagittal 切片。它可以與我們之前討論的切片投影方法相結合,如下圖所示的兩個影像集,其中藍線突出顯示了冠狀面投影的限制

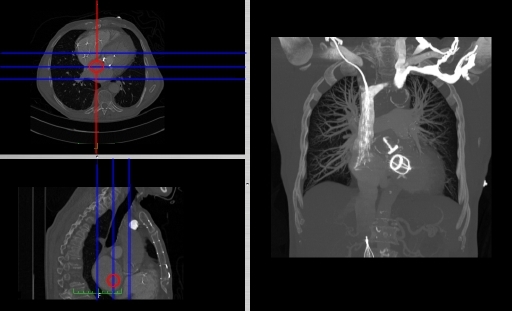
- 斜面重建
- 透過在體素資料中定義傾斜平面可以實現斜面 MPR,如下圖所示

- 在這裡,平面可以在軸向影像(左上角的紅線)中定義,並且可以為重建的平面(右側)顯示最大強度投影(使用的限制由藍線突出顯示),例如。當試圖生成透檢視時,這種技術很有用,在這種情況下,三維結構的視覺化因重疊的解剖細節而變得複雜。
- 曲線重建
- 曲線 MPR 可用於重建更復雜的透檢視,如下圖所示

- 在這裡,可以在軸向影像(左面板)中定位一條曲線(以綠色突出顯示),以定義一條延伸到 z 方向的體素資料的彎曲曲面,並且可以將來自該資料的體素重建成二維影像(右面板)。請注意,可以生成比圖中所示更復雜的曲線,例如,可以隔離主要血管的三維走向,或者可以將 CT 頭部掃描平面化以進行正畸應用.
- 3D 多平面重建
- MPR 主題的最後一個變體是生成一個三維顯示,顯示所有三個正交投影的組合,以便定義的感興趣點定位平面的交點,如下圖所示

- 為了說明目的,交點位於上述圖形中體素資料的中心。它通常可以使用互動式控制元件放置在 3D 資料中的任何點。此外,通常可以互動地操縱用於旋轉序列的透檢視,以改善對感興趣區域的視覺化。請注意,上面圖示的影像序列是可以透過這種方式生成的大量透檢視中的一種。還要注意,切片投影(例如 MIP)可以與這種形式的顯示相結合,以提供對感興趣特徵的額外透檢視。
最大強度投影
[edit | edit source]我們在軸向投影的背景下描述了最大強度投影 (MIP),其中最大體素值是透過投影切片厚度平行執行的直線確定的。當這種計算應用於圍繞體素資料進行連續角度的投影時,可以生成一系列這樣的影像。一個簡單的序列是圍繞水平平面旋轉 360 度,如下圖左側面板所示,其中最大強度投影到患者周圍每 9 度,並將產生的 40 個影像編譯成一個重複的時序(例如 電影)序列

請注意,3D MIP 從 CT 掃描的衰減最強的區域獲取其資訊(因為CT 數值直接取決於線性衰減係數),因此描繪了骨骼、對比介質和金屬,而周圍的衰減較低的組織幾乎沒有資訊。還要注意,持續觀看旋轉 MIP 序列會產生令人不安的效果,其中旋轉方向似乎週期性地反轉——這可能是感知振盪的一個方面。上述圖形中右側面板中圖示的透視 MIP 可以透過提供可用於指導持續視覺檢查的空間線索來減少這種侷限性。
透視投影可以透過從用於生成平行投影的平行線更改為體素線來生成,這些體素線從體積後面某個明顯點發散,距離使得顯示器的觀看者可以將影像資料的更近特徵視覺化為相對大於更深特徵——參見下圖

體繪製
[edit | edit source]體繪製可以應用於體素資料,採用上面針對 MIP 描述的連續旋轉方式,如下圖所示的結果

請注意,可以增強體繪製的對比度,例如,透過體素值進行閾值化,以消除低衰減表面,如下圖所示

還要注意,可以改變顏色查詢表 (CLUT) 以突出顯示特別感興趣的特徵,如下面的影像集所示

以下示例影像說明了不透明度表的影響
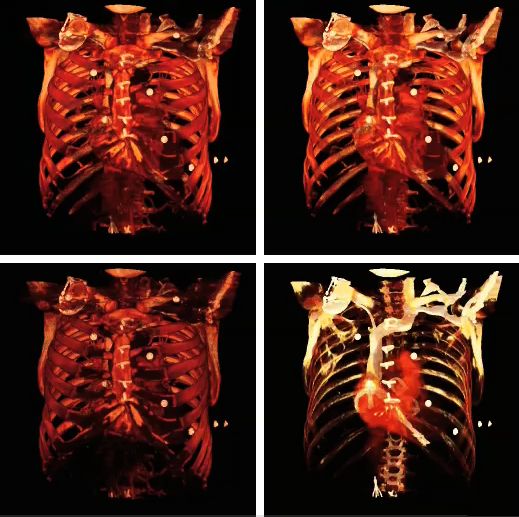
以下顯示了各種陰影設定對體繪製的影響
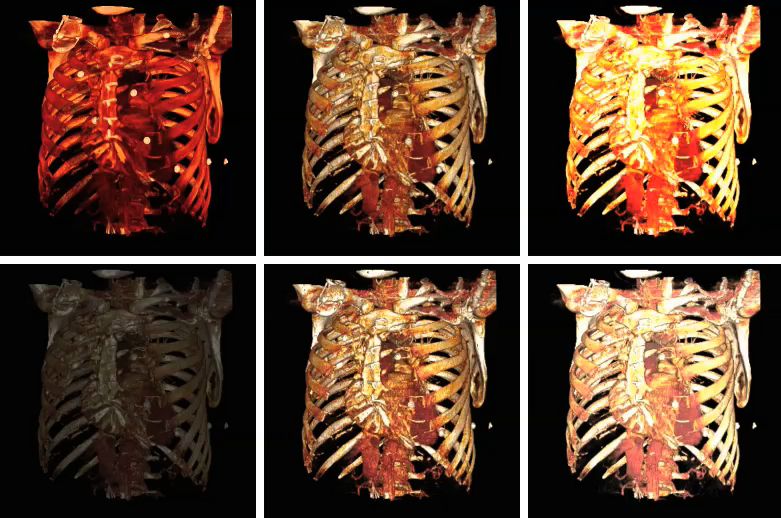
上面影像使用的陰影設定如下
| 影像 | 環境係數 | 漫射係數 | 鏡面反射係數 | 鏡面反射功率 |
|---|---|---|---|---|
| 左上角 | 0.15
|
0.9
|
0.3
|
15.0
|
| 中間頂部 | 0.75
|
0.9
|
0.3
|
15.0
|
| 右上角 | 0.15
|
0.1
|
0.3
|
15.0
|
| 左下角 | 0.15
|
0.9
|
1.2
|
15.0
|
| 中間底部 | 0.15
|
0.9
|
0.1
|
1.0
|
| 右下角 | 0.15
|
0.9
|
0.6
|
1.0
|
關於體繪製要說明的最後一個特徵是,可以應用 3D 編輯技術,以從計算中排除不需要的特徵並暴露內部結構。這在以下圖形中有所說明,其中正交框架的平面可以移動以從六個方向裁剪體素資料。

表面渲染也稱為陰影表面顯示 (SSD),它涉及從 3D 資料中具有相似體素值的區域生成表面,如下面的左側面板中顯示的 SPECT 肺灌注掃描所示。

該過程涉及基於以下事實顯示可能存在於 3D 體素資料中的表面:物體的邊緣可以預期具有相似的體素值。一種方法是使用灰度閾值技術,其中一旦在投影線上遇到閾值,就會提取體素——請參見以下圖表。然後使用三角形對提取的體素進行鑲嵌,如上圖右側面板所示——並且使用恆定值填充三角形,並在模擬固定虛擬光源的效果的基礎上應用陰影——如上圖左側面板所示。

可以將不透明度表應用於結果,以便還可以視覺化內部特徵的表面。例如,在下圖中從 CT 掃描中識別出兩個表面,其中來自骨表面的體素值以不透明的黃色編碼,組織表面以透明的紅色陰影編碼。

在下圖中顯示了使用不透明度表的第二個示例。在這裡,使用區域增長技術對來自患者氣道軸向 CT 資料進行分割,然後使用表面渲染對結果進行處理,完全不透明,如左側面板所示,並使用降低的不透明度 (30%),如右側面板所示。

注意,當降低不透明度時,可以辨別每隻肺的內部特徵。還要注意,繼續檢視這種型別的透明度顯示會產生影像旋轉的明顯反轉,類似於上面提到的 3D MIP。克服此類問題的一種方法是例如分割每隻肺並混合結果,如以下圖所示。

我們將透過考慮 3D 視覺化的一個應用來結束本章,該應用整合了我們在本華夏公益教科書中描述的許多影像處理技術。我們將在嘗試視覺化肺栓塞 (PE) 的特徵性失配時,使用來自患者肺通氣 (V) 和肺灌注 (Q) 研究的兩個 SPECT 掃描。我們將考慮的應用程式稱為subFusion 處理,因為它涉及影像減法和影像融合技術。
再次注意,SPECT 研究是使用淹沒技術生成的,其中灌注掃描在使用產生掃描之間約 5:1 的相對計數率的給藥活性後立即獲取通氣掃描。因此,第一個影像處理步驟是校正灌注掃描的背景通氣活性。
由於在這種情況下通氣示蹤劑是使用氣霧劑給藥的,我們可以簡單地假設它的生物分佈在這兩個掃描中是相當相同的。此外,由於掃描是在使用99mTc 放射性同位素相隔約 15 分鐘後獲取的,我們可以假設放射性衰變的影響可以忽略不計。因此,基於這些假設,我們可以簡單地從灌注堆疊中減去通氣堆疊,以隔離我們將稱為“純灌注”掃描的內容。
第二步是透過將通氣堆疊乘以一個因子來歸一化兩個掃描,使得兩個堆疊中的平均計數(例如)相似。
- 現在我們可以比較蘋果和蘋果了!
由於 PE 失配很可能來自肺部的區域,這些區域在通氣掃描中包含計數,而在灌注掃描中相對缺乏此類計數,因此我們可以將“純灌注”堆疊從通氣堆疊中減去,作為第三個影像處理步驟,以隔離任何此類差異作為正值特徵。
最終的影像處理步驟是將此差異堆疊與“純灌注”掃描一起進行體積渲染,並將結果混合,如以下影像所示。

以下圖示出了所涉及的步驟。請注意,為了簡單起見,圖中省略了一些次要過程,例如 CLUT 選擇、相對不透明度調整和對比度增強。還要注意,在患者在兩次 SPECT 獲取之間發生移動的情況下,可能需要在程式開始時包含影像配準步驟。

最後一點需要注意的是,與 SPECT 影像相比,分割的 CTPA 影像中患者肺的尺寸更大。這是因為 CTPA 研究是在單次屏氣下獲取的,而 SPECT 研究是在患者在伽馬相機旋轉期間安靜呼吸的情況下獲取的。因此,三組影像的配準無法直接進行,需要應用空間扭曲和其他技術,不幸的是,這些技術超出了我們這裡處理的範圍。
