結構生物化學/有機化學/純化方法

重結晶是一種純化方法,涉及將固體溶解在熱溶劑中,過濾加熱的溶液或混合物,形成晶體,以及分離結晶化合物。為了進行重結晶,必須利用化合物在熱溶劑中的溶解度。在較高溫度下,飽和溶液通常比相同溶質/溶劑對在較低溫度下含有更多的溶質;因此,當溫熱的飽和溶液冷卻時,溶質會沉澱出來。換句話說,較高溫度下的溶液將具有更多的溶解固體,並且當它冷卻時,溶質將返回到其固相,形成沉澱物。正在重結晶的固體中的雜質通常比被純化的物質的濃度低得多,因此當混合物冷卻時,雜質仍然留在溶液中,而高濃度的產物結晶。
溶質從溶液中形成晶體是一個選擇性過程,因為只有以正確速度移動的固體,並在適當的濃度和溶劑條件下,才能形成幾乎完美的晶體材料,因為只有具有正確形狀的分子才能適合晶格。重結晶純化化合物是因為將不純固體溶解在合適的熱溶劑中會破壞不純化合物的晶格,並且從冷溶劑中重結晶會選擇性地產生新的、更純的晶格。緩慢冷卻飽和溶液有利於形成純晶體,因為不合適的雜質分子有時間返回溶液。緩慢形成的晶體比快速形成的晶體更大(不總是這樣)並且通常更純淨,因為快速晶體形成會將雜質捕獲在晶格中,因為它們只是被結晶溶質包圍。重結晶最重要的方面是選擇溶劑,因為溶質在熱溶劑中應具有最大溶解度,而在冷溶劑中應具有最小溶解度。溶質和溶劑的關係可以用“相似相溶”來最好地描述。這意味著非離子化合物通常僅在它們可以透過氫鍵與水分子結合時才溶於水。烴和烷基鹵化物實際上不溶於水,而羧酸和醇類通常從水溶液中重結晶。在微型重結晶實驗中,遵循幾個步驟來完成純化過程。
- 要重結晶的固體必須首先稱重,然後溶解在合適的熱溶劑中。
- 必須使用重力過濾法過濾固體雜質。
- 然後將熱的重結晶混合物放置一旁冷卻至室溫。
- 冷卻至室溫後,將溶液進一步冷卻,將其放入冰水浴中 10-15 分鐘,以允許進一步重結晶。
- 為了收集晶體並完成重結晶,必須透過真空過濾收集晶體。
透過重結晶進行純化的一個關鍵因素是瞭解溶解度。為了成功進行重結晶過程,混合物必須具有一些重要的溶解度特性。一種溶劑必須在所有溫度下都可溶。下一個溶劑必須在低溫下可溶。另一個溶劑必須在高溫下可溶,在低溫下不可溶。
這是一個簡單的插圖,解釋瞭如何進行純化過程。
藍色正方形在所有溫度下都可溶,橙色圓圈在所有溫度下基本上都不溶,綠色三角形在高溫下可溶,在低溫下不可溶。
- 1. 加熱:如果我們加熱包含正方形、圓形和三角形的混合物,正方形將已經處於溶液中,我們可以將其加熱到綠色三角形溶解的程度。然後我們只剩下不溶的圓圈。
- 2. 過濾:然後我們可以過濾含水溶解的溶液,一旦我們將它分離,我們只剩下三角形和正方形處於溶液中,而圓圈則留在前一個容器中。
- 3. 冷卻:當新分離的混合物冷卻時,三角形將開始再次結晶,因為它在低溫下不溶,但正方形將仍然留在溶液中,因為它在所有溫度下都可溶。
- 4. 我們分離含水層(三角形),我們剩下我們感興趣的化合物,即三角形。

等電聚焦是一種電泳蛋白純化過程,其中蛋白質根據其等電點進行分離。蛋白質的等電點,即pI,是在蛋白質不帶淨電荷時的特徵 pH 值。蛋白質的淨電荷由構成蛋白質的側鏈的酸度或鹼度決定。如果蛋白質的酸性基團多於鹼性基團,則該蛋白質將具有非常低的 pH 值,被認為是酸性的。如果蛋白質在其側鏈中具有比酸性基團更多的鹼性基團,則蛋白質的總電荷將使其 pH 值高得多。等電聚焦利用以下步驟利用這些特性
- 建立一個凝膠,凝膠內具有線性 pH 梯度
- 將蛋白質樣品插入凝膠中
- 施加電場,一端為陽極 (+),另一端為陰極 (-)
- 留出時間讓蛋白質根據其淨電荷遷移到其中性 pI
凝膠的線性 pH 值允許樣品任意新增,因為環境的 pH 值與電場相結合將迫使蛋白質移動,而不管它們在凝膠中的初始位置如何。蛋白質只有在施加電場後才開始遷移。在施加電場後,蛋白質會朝著與它們電荷相反的端子移動,在遷移過程中聚集或釋放質子,直到它們達到其中性等電點。例如,假設所有蛋白質樣品都已新增到梯度的中性 pH 位置,其中 pH=7。當電場最終施加時,蛋白質會根據其淨電荷遷移。如果蛋白質的等電點為 2,則在 pH 值為 7 時,蛋白質的氫離子比它為中性(即達到其等電點)所需的氫離子少。這使蛋白質呈負電性,因此它會朝著陽極 (+) 移動,在穿過梯度到更低的 pH 值時吸收質子。當蛋白質最終吸收了足夠的質子使其呈中性時,蛋白質將不再具有淨電荷,並在其等電點停止遷移。
等電聚焦允許根據不同的蛋白質特徵(pI)進行蛋白質純化。因此,具有類似特徵(例如分子量)的蛋白質可以透過其獨特的 pI 在相當短的時間內進行純化和分離。[1]
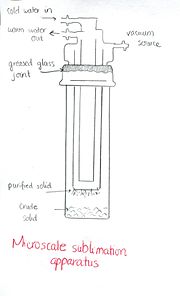
昇華是指物質直接從固相轉變為氣相,而不形成中間液相的過程。乾冰就是一個例子,它從二氧化碳的固體形式直接轉化為二氧化碳氣體。在實驗室中,昇華只能在滿足四個要求後才能用於純化有機化合物。
- 該化合物必須在不熔化的條件下汽化
- 它必須足夠穩定,能夠在不分解的情況下汽化
- 該化合物的蒸汽必須能夠凝結回固體
- 化合物內的雜質也不升華。
昇華裝置包括一個外容器和一個內容器。外容器容納要純化的樣品,並連線到真空系統。被稱為冷指的內容器提供了一個冷表面,汽化的化合物可以在該表面上重新凝結成固體。為了進行昇華,要昇華的樣品必須放入一個濾瓶中。接下來,將一根內管放入燒瓶中,開啟真空系統。之後,使用沙浴輕輕加熱昇華燒瓶,同時在內管中裝滿冰。在昇華過程中,物質會從外容器底部消失,然後重新出現在內試管的冷外表面上。這是因為化合物在達到其昇華溫度時會汽化,然後由於冷卻而在冷指上重新凝結。完成後,可以取出內試管,刮掉純淨固體並進行分析。
在昇華過程中,需要注意不純化合物和冷凝管之間的距離。昇華裝置的各部分需要足夠靠近以避免分解,但又要足夠遠以防止汙染。較大的距離意味著需要更高的溫度才能保持化合物以氣態形式存在,這會導致化合物分解。較小的距離會導致雜質很容易接觸到冷凝管上純化的化合物。如果不考慮距離,純化可能無效。[2]
蒸餾
[edit | edit source]蒸餾用於分離雙組分混合物,而氣相色譜法用於識別組分化合物。蒸餾是一種根據化合物蒸汽壓和沸點分離化合物的技術。當兩種不同的化合物被加熱時,一種可能比另一種在更低的溫度下沸騰。透過將沸點較低的化合物的蒸汽與另一種化合物分離,可以將蒸汽從液體中分離出來並重新冷凝,從而有效地分離兩者。透過連續蒸餾,可以實現高度的純化。一次進行的蒸餾稱為簡單蒸餾。雖然可以透過多次簡單蒸餾實現高效率,但這將是繁瑣的並且需要大量的初始樣品量。然而,精餾簡化了這種重複蒸餾,因為它提供了連續分離。精餾柱用於提供廣闊的表面積,以便蒸汽上升和冷凝液下降之間的熱交換;透過遞迴機制,上部蒸汽在更易揮發的化合物中更純淨,液體在更難揮發的化合物中更純淨。分離程度取決於化合物的不同沸點以及蒸餾速度、絕緣和柱效率。透過延長蒸餾時間,可以達到熱平衡並獲得更高的純度。同樣,絕緣可以防止熱量損失以保持初始條件,而柱效率決定了可以發生多少個蒸餾“口袋”。
薄層色譜法 (TLC)
[edit | edit source]薄層色譜法 (TLC) 是一種簡單快捷的分離和鑑別混合物中成分的方法。原則上,混合物中不同的成分具有不同的溶解度,並且對吸附劑的吸引力強度也不同。該方法利用了這一原理,將待分析的混合物在塗有薄層固體吸附劑的板上進行,然後將板浸入溶劑中。混合物中的成分將以不同的速度緩慢地向上移動,直到它們達到該特定溶劑和吸附劑組合的最大分離度。混合物分離成不同的彩色斑點後,將板乾燥並檢查成分。
技術
1. 選擇用於分析混合物的溶劑,然後將其倒入燒杯中,深度小於 0.5 釐米。整個過程在燒杯中進行,並在頂部蓋上表面皿,以防止溶劑蒸汽逸出。
2. 製備 TLC 板。TLC 板由薄層吸附劑製成,通常是矽膠或氧化鋁。在板的底部附近,用鉛筆在板上畫一條線。這條線將是您點待分析混合物的起點。
3. 將板放入燒杯中,使只有板的底部浸入溶劑中。
4. 當溶劑透過毛細管作用向上移動並經過塗抹的點時,混合物中的一些成分將由於其在溶劑中的溶解度及其對板的吸附強度而以更快的速度移動。
5. 板上將出現不同的彩色斑點分離。如果斑點沒有顏色,則使用紫外燈觀察板。
為了識別存在的化合物,從板上測量溶劑移動的距離和各個斑點移動的距離。使用這些測量結果,透過以下公式獲得保留因子 Rf
Rf = (Distance traveled by the compound)/(Distance traveled by the solvent)
從 Rf 值可以預測化合物的極性。此外,該值可用於比較兩種化合物。如果兩種物質具有相同的 Rf 值,則它們很可能是相同的化合物。否則,它們肯定是不同的化合物。
參考文獻
[edit | edit source]- ↑ Andrews, A.T. (1986). 電泳:理論、技術以及生化和臨床應用(第二版)。牛津大學出版社,牛津。
- ↑ Mohrig, Jerry R. “有機化學技術”。2010,W.H. Freeman 和公司
Mohrig, Jerry R. 有機化學技術。2006,W.H. Freeman 和公司
有機化學實驗室,化學 143A

