結構生物化學/相圖
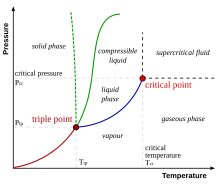
相圖是一個圖表,它有助於定義物質處於固態、液態和氣態時的條件。圖表的三個邊界線表示相之間的平衡關係:熔化曲線、汽化曲線和昇華曲線。圖表上還有兩個不同的點:三相點和臨界點。為了更好地定義這些術語,可以觀察圖片圖表。紅線是固態到氣態之間的轉變,也稱為昇華曲線。綠線是固態到液態的轉變,也稱為熔化曲線。藍線是液態到氣態的轉變,稱為汽化曲線。三條線相交的點是三相點。在這個溫度和壓力下,三個相:固態、液態和氣態可以共存。臨界點是物質能夠觀察到的蒸汽/液體平衡的最高壓力和溫度條件。
任何超過最高壓力和溫度的條件都會變成一個沒有明確相界限的區域。通常,當汽化來自恆定 T 下的減壓時,相被認為是液體,如果冷凝來自恆定 T 下的降溫,則相同情況適用於氣體。由於此過程不能應用於任何一種情況,因此超過最高 P 和 T 的區域可以被認為是超臨界的,並且是流體區域。
超臨界流體被定義為高於其臨界溫度 (Tc) 和臨界壓力 (Pc) 的物質。臨界點表示物質以蒸汽和液體平衡狀態存在的最高溫度和壓力。超臨界流體是高度壓縮的氣體,以一種引人入勝的方式結合了氣體和液體的特性。超臨界氙氣、乙烷和二氧化碳等流體在合成化學和分析化學中都提供了各種不尋常的化學可能性。超臨界流體對大多數溶質的溶解能力類似於輕質烴。然而,氟化化合物通常比在烴中更易溶於 scCO2。這種溶解度提高對於聚合反應很重要。

雖然相圖通常被視為顯示物質在特定條件下的狀態的圖,但這種簡單的工具可以用於分析其他複雜材料。例如,從相圖中獲得的資訊可用於討論蛋白質晶體學。該圖表示蛋白質晶體學所需的蛋白質和沉澱劑濃度。紅線稱為溶解度線,它將過飽和條件與未飽和條件明顯分開,而過飽和條件是蛋白質結晶所需的條件。相圖的過飽和部分包含三個部分:亞穩態、不穩定和沉澱。
亞穩態-這裡的晶體可以從晶種長大,但不能成核。蛋白質和沉澱劑濃度較低,聚集事件較少。這個區域表示通常結晶發生速度太慢的濃度。
不穩定-這裡的晶體也可以從晶種長大,但它們可以成核。蛋白質和沉澱劑濃度較高,聚集事件更多。這個區域也稱為成核區或結晶區,更有利於晶體的形成。
沉澱-蛋白質通常以聚集體或沉澱物形式出現,不適用於晶體學。該圖的這一部分顯示了不太有利的條件,因為聚集和沉澱比結晶發生得快得多。
成核:建立核心的過程。
聚集:蛋白質的團聚或聚集。
相圖和蛋白質結晶之間的聯絡是溶解度曲線(紅線)的位置。如前所述,晶體只能在過飽和溶液中形成,瞭解溶解度曲線的位置可以促進晶體生長,用於 X 射線晶體學。雖然需要晶體來確定溶解度曲線,但透過各種試驗可以找到適合晶體形成的濃度。透過這種資料積累,晶體可以用作最佳化蛋白質結晶條件的指南。
該相圖也被使用,因為它揭示了溶液中多種組分之間的相互作用。此類相互作用的例子是定義蛋白質之間吸引力的液-液相分離 (LLPS),這是蛋白質結晶的必要特徵。這種吸引力在 LLPS 中得到了很好的定義。可以從相圖中提取的其他資料包括焓(來自 LLPS)和熵(來自溶解度曲線)在液態和固態中的蛋白質。此外,新增劑可以改變相圖的曲線,從而提供有關新增劑效應以及它如何與蛋白質分析物相互作用的資料。它也可以用於預測蛋白質結晶所需條件,這對於結晶過程來說是理想的,減少了試錯,並提高了結晶率。
向蛋白質溶液中新增沉澱劑的結果是形成液滴。這些液滴有時被稱為油或凝聚體,可以在改變溫度、pH 值和其他溶液條件變化時觀察到。液滴通常含有高濃度的蛋白質,當受到更高的力(重力)影響時,液滴會從溶液的其餘部分分離出來。其結果是溶液中的兩個液相。整個過程稱為液-液相分離。LLPS 很有用,因為高濃度的蛋白質有助於將飽和度提高到過飽和狀態,從而增加了結晶率。
