結構生物化學/酶/輔因子
輔因子是無機和有機化學物質,它們在反應催化過程中輔助酶。輔酶是大多數是水溶性維生素磷酸化衍生物的非蛋白質有機分子;它們與蛋白質結合以產生活性脫輔酶。脫輔酶是缺少其正常功能所需的輔因子(s)的酶;酶與輔酶的結合形成全酶。全酶是脫輔酶的活性形式。


輔因子可以是金屬或小有機分子,它們的主要功能是協助酶活性。它們能夠幫助完成酶自身無法完成的某些必要反應。它們被分為輔酶和輔基。全酶是指一種催化活性酶,它由脫輔酶(沒有輔因子的酶)和輔因子組成。輔因子有兩類:金屬和小有機分子,稱為輔酶。輔酶是通常從維生素中獲得的小有機分子。輔基是指與酶緊密結合的輔酶,而輔基是指鬆散結合的輔酶,它們像底物和產物一樣被釋放。鬆散結合的輔酶與底物不同,因為相同的輔酶可以被不同的酶使用,以實現適當的酶活性。
通用公式
金屬離子是常見的酶輔因子。一些酶被稱為金屬酶,如果沒有活性位點中結合的金屬離子,它們就不能發揮作用。在日常營養中,這種輔因子作為必需微量元素髮揮作用,例如:鐵(Fe3+)、錳(Mn2+)、鈷(Co2+)、銅(Cu2+)、鋅(Zn2+)、硒(Se2+)和鉬(Mo5+)。例如,Mg2+用於糖酵解。在將葡萄糖轉化為葡萄糖-6-磷酸的第一步中,在使用 ATP 生成 ADP 和一個磷酸基團之前,ATP 與 Mg2+ 結合,這會穩定另外兩個磷酸基團,使其更容易釋放出一個磷酸基團。在一些細菌中,如Azotobacter屬和Pyrococcus furiosus,金屬輔因子也被發現起著重要作用。輔因子作用的一個例子是碳酸酐酶的鋅介導功能或限制性內切酶的鎂介導功能。
輔酶是一種小型的、有機、非蛋白質分子,它在酶之間傳遞化學基團。它是酶的輔因子,並且不是酶結構的永久部分。有時,它們被稱為輔底物,並被認為是鬆散地結合到酶上的底物。在代謝中,輔酶在基團轉移反應中起作用,例如 ATP 和輔酶 A,以及氧化還原反應,例如 NAD+ 和輔酶 Q10。輔酶經常被消耗和迴圈利用。化學基團不斷被酶新增和分離。ATP 合酶磷酸化並將 ADP 轉換為 ATP,而激酶以持續的速率將 ATP 去磷酸化回 ADP。輔酶分子大多來源於維生素。它們也通常由核苷酸製成,例如三磷酸腺苷和輔酶 A。
透過對輔酶活性和其對酶的結合作用的進一步研究,可以更多地揭示酶在構象和功能上的變化方式。一個例子是 MAPEG 組的跨膜整合酶。這些酶在親脂性底物的催化轉化中至關重要,這些底物參與花生四烯酸衍生信使的產生和異生物質解毒。透過使用與 MAPEG 酶的輔因子谷胱甘肽類似的結合去垢劑,揭示了針對親脂性底物的新的活性位點;因此,進一步的研究可以揭示這些底物如何結合到酶的第二種形式[1]。

煙醯胺腺嘌呤二核苷酸是一種來源於維生素B3的輔酶。在 NAD+ 中,分子的功能基團只是煙醯胺部分。NAD+ 能夠攜帶和轉移電子,在氧化還原反應中充當氧化劑。它也作為蛋白質翻譯後修飾中 DNA 連線酶的底物,其中反應從蛋白質中去除乙醯基。此外,在糖酵解和檸檬酸迴圈中,NAD+ 氧化葡萄糖並釋放能量,然後透過還原為 NADH 將能量轉移到 NAD+。NADH 後來透過氧化磷酸化釋放額外的電子,生成 ATP,這是人類每天使用的能量來源。除了分解代謝反應之外,NADH 還參與合成代謝反應,例如糖異生,並且它還有助於大腦中神經遞質的產生。
黃素腺嘌呤二核苷酸是一種輔基,與 NADH 一樣,在細胞呼吸中充當還原劑,並將電子傳遞給電子傳遞鏈。
-
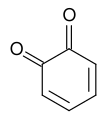
1,2-苯醌
-
1,4-苯醌
-
蒽醌
具有完全共軛芳香環的化合物,兩個氧原子以羰基形式結合到這些環上(即二酮)。醌的結構使它們能夠形成有色物質。它們存在於細菌、真菌和某些植物中的色素中,並賦予它們特徵顏色。此外,它們被用於製造不同的工業染料。在生物系統中,它們在電子傳遞鏈中充當電子受體(氧化劑),例如光合作用和有氧呼吸中的電子傳遞鏈。許多天然或合成的喹啉表現出生物學或藥理學活性,一些甚至表現出抗腫瘤活性。
輔酶 A,由泛酸 ATP 合成,在代謝反應中充當醯基載體,用於在代謝反應中轉運功能基團,例如乙醯基(乙醯輔酶 A)或硫酯,例如脂肪酸氧化(脂肪酸的合成)和檸檬酸迴圈(細胞呼吸)。它還將脂肪酸從細胞質轉運到線粒體。除了在代謝中的轉運作用外,CoA 本身也是一個重要的分子。例如,CoA 是 HMG-CoA 的重要前體,HMG-CoA 是膽固醇和酮體代謝合成的重要酶。此外,它將乙醯基新增到乙醯膽鹼的結構中,乙醯膽鹼是一種重要的神經遞質,負責誘導肌肉收縮。
維生素A可以細分為兩個分子,維生素A1(視黃醇)和維生素A2(脫氫視黃醇)。視黃醇是活性最高且最常見的形式。維生素A具有一個大的共軛鏈,作為該分子的反應位點。與大多數輔因子不同,維生素A在回到其原始形式之前會經歷一系列化學變化(氧化、還原和異構化)。維生素A的電子可以從軌道轉移的能力,使其成為捕捉光能的理想分子。因此,維生素A負責將光能傳遞到眼球中的化學神經衝動。維生素A還用於生長健康的新的細胞,例如皮膚、骨骼和頭髮。它維持泌尿道、腸道和呼吸系統的內壁。此外,維生素A對於生殖功能是必需的,例如精子和卵巢的生長和發育。
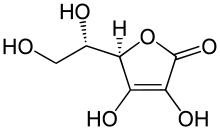
維生素C
[edit | edit source]維生素C也稱為抗壞血酸,在大多數植物和動物中都很豐富,除了靈長類動物、豚鼠、蝙蝠和一些鳥類。儘管人類無法合成抗壞血酸,但它在許多生物合成途徑中是必不可少的,例如合成膠原蛋白。缺乏會導致一種稱為壞血病的疾病。維生素C有助於調節免疫系統並減輕疲勞肌肉引起的疼痛。它也是製造膠原蛋白和去甲腎上腺素所必需的。維生素C也是一種抗氧化劑,可以透過刺激體內的白細胞來增強免疫系統。維生素C還有助於改善皮膚、牙齒和骨骼。
維生素B1
[edit | edit source]維生素B1也稱為硫胺素或硫胺素二磷酸(TPP),是克雷布斯迴圈和將丙酮酸轉化為乙醯輔酶A(代謝中檸檬酸迴圈中使用的重要分子)中氧化脫羧作用的輔因子。它在人類飲食中廣泛存在,在麥芽和酵母中特別有效。它的功能來源於一個噻唑環,該環透過共振來穩定電荷和電子轉移。
維生素B2
[edit | edit source]維生素B2被稱為核黃素。維生素B2是黃素腺嘌呤二核苷酸(FAD)和黃素單核苷酸(FMN)的前體,它們是用於氧化底物的輔酶。FAD包含核黃素和腺嘌呤。FMN包含核黃素,這就是為什麼它被稱為單核苷酸。
維生素B3
[edit | edit source]維生素B3是煙酸或煙酸,化學式為C5H4NCO2H。維生素B3是NADH、NAD+、NADP+和NADPH的前體,它們是存在於所有活細胞中的輔酶。NAD+和NADP+是氧化劑。NADH和NADPH是還原劑。
維生素B6
[edit | edit source]維生素B6是輔酶磷酸吡哆醛(PLP)的前體,它在某些氨基酸轉化中是必需的,包括轉氨基、脫氨基和脫羧作用。
維生素B12
[edit | edit source]維生素B12是具有這種維生素活性的相關化合物的一類名稱。這些化合物含有稀有元素鈷。人類無法合成B12,必須從飲食中獲取。
維生素H
[edit | edit source]維生素H也稱為生物素,是一種羧基載體;它結合CO2並將CO2攜帶,直到CO2在羧化酶反應中被捐贈。它是一種水溶性維生素,在脂肪酸和亮氨酸的代謝中很重要。缺乏會導致皮炎和脫髮,因此成為化妝品中的熱門成分。
維生素K
[edit | edit source]維生素K是血液凝固和Ca2+結合過程所必需的。維生素K可以在腸道中的細菌合成。維生素K是催化蛋白質中谷氨酸側鏈γ-碳的羧化所需的。
非酶促輔因子
[edit | edit source]輔因子在生物學領域也被廣泛用於指啟用、抑制或蛋白質發揮功能所需的分子。例如,與受體蛋白結合並激活受體蛋白的配體,例如激素,被稱為輔因子或共啟用因子,而抑制受體蛋白的分子被稱為共抑制因子。
共啟用因子可以透過穩定 RNA 聚合酶全酶的形成來增強轉錄起始,從而使啟動子更快地清除。
共抑制因子可以透過募集組蛋白脫乙醯基酶來抑制轉錄起始,組蛋白脫乙醯基酶催化從賴氨酸殘基去除乙醯基。這會增加組蛋白的正電荷,從而增強組蛋白與 DNA 之間的相互作用,使後者更難以被轉錄。
參考文獻
[edit | edit source]- Dewick,Paul。藥物天然產物:生物合成方法。第 3 版。英國西薩塞克斯:Wiley,2009 年。32-34。印刷。
- von Heijne,G 和 Rees,D(2008 年)。《結構生物學最新觀點》。愛思唯爾有限公司。
- ↑ von Heijne G,Douglas R:膜:閱讀行間字。結構生物學最新觀點 2008,18:403-405