有機化學/環烷烴
環烷烴是一種具有環或環狀結構的常規烷烴。例如環己烷,它是一個由 6 個碳原子組成的環,每個碳原子連線到 2 個氫原子 (C6H12)。
我們在本書的烷烴單元中簡要討論了環烷烴,但在本單元中,我們將更詳細地介紹環烷烴和環烯烴。這些結構有一些獨特的性質,因此值得特別關注。
由於環狀結構,環烷烴不具備普通烷烴所具有的旋轉自由度。立體化學在運動的限制以及在某些情況下反應的限制方面起著非常重要的作用。這些限制往往更多地是由於環狀結構本身,而不是由於此類烷烴中缺乏旋轉自由度。
一個很好的例子是對E2消除反應的限制,我們將在本書的後面部分討論。

上面顯示的前四個簡單環烷烴的影像表明,每個碳原子連線了 2 個氫原子。如您所見,另外 2 個鍵連線到相鄰的碳原子。雖然這些形狀顯示了基本的二維、自上而下的形狀,但只有環丙烷和環丁烷的所有碳原子都在同一平面上。環戊烷和環己烷以及更高環烷烴都具有三維幾何形狀。環己烷尤為重要,我們將在後面單獨討論。

更常見的是,環烷烴,像許多其他有機結構一樣,被繪製成不標記碳原子和氫原子。環戊烷和環己烷(見上文)通常分別繪製成五邊形和六邊形。
環烷烴的命名類似於烷烴。最小的環烷烴是“環丙烷”,因此您可以想象,這是一個由 3 個碳原子組成的環。如果環烷烴上的碳原子數量多於其任何取代基(即連線到環烷烴上的碳原子上的碳鏈)上的碳原子數量,則基本名稱字首為“環”,其餘名稱與具有相同碳原子數量的烷烴相同。

如果,如上圖所示,環烷烴的碳原子數量少於它連線的碳鏈的碳原子數量,則最長的碳鏈是主要的,而環狀部分接收取代基“-yl”字尾並在主要名稱前新增字首。因此,名稱 1-乙基丁基環戊烷雖然在技術上是準確的描述,但不是正確的名稱。

取代環烷烴中碳原子的編號相當簡單。如果只有一個取代基,則為 1 碳。如果有多個取代基,則編號順時針或逆時針進行,使得 1 之後的最低編號對應於取代基最少(或至少)的碳原子。我知道這聽起來很棘手,所以我們來看一下左邊的例子,3-氯-1,1-二甲基環己烷。具有氯鍵的碳原子是取代基最少的碳原子,因此它得到 1 之後的最低編號,而 1 則對應於最靠近具有多個取代基的碳原子的碳原子。因此,1 應用於甲基。取代基仍然按字母順序排列,如第二個例子 2-溴-3-氯-1,1-二甲基環己烷所示。
具有 4 個單鍵的碳原子希望這些鍵處於 109.5° 的四面體角。1885 年,阿道夫·馮·拜耳提出,由於碳原子更喜歡這個角度,因此只有 5 元環和 6 元環才能形成。拜耳犯了一個錯誤,就是用二維思維來思考並假設所有環都是平面的。事實上,只有環丙烷和環丁烷是平面的,導致它們的鍵角分別為 60° 和 90°。但在一段時間內,人們認為這些較小的環烷烴無法合成,而超過 6 個碳原子的環烷烴會產生張力,因為它們的鍵角將遠遠超過 109.5° 的偏好角度。

在上圖中,再次展示了前四個簡單環烷烴,但這次顯示了三維模型。請注意環戊烷是如何有 4 個碳原子在同一個平面上,而第 5 個碳原子稍微偏離平面,使其呈現出開啟的信封形狀。
事實上,大於 3 個碳原子的環具有減輕這種鍵張力的三維形狀,但重要的是要注意鍵張力確實會影響穩定性。對於環丙烷和環丁烷,張力能約為 110 kJ/mol。環丁烷可以進入“褶皺”形式,略微減輕了一些扭轉張力。環戊烷是非平面的,可以消除一些張力,只有大約 25 kJ/mol 的張力。環己烷由於其椅式構象,可以保持完美的四面體角,從而沒有張力。隨著環尺寸進一步增加,可以避免鍵角張力,但會引入一些重疊張力,反之亦然,因此會存在一些張力,但其中張力最大的,環壬烷,只有大約 50 kJ/mol 的張力。環張力在高達 13 個成員的環尺寸中普遍存在。之後,有足夠的碳原子可以完全消除環張力。

但鍵角張力並不是環張力中唯一涉及的問題。扭轉張力也是一個因素。當環中的氫鍵相互重疊時,就會產生額外的張力。在環丙烷的情況下,氫原子相互重疊,極大地增加了張力。事實上,這是環戊烷中大部分張力的原因。環戊烷的鍵角非常接近 109.5°,但由於其 4 個碳原子是平面的,因此存在扭轉張力,使其不太穩定。從上圖中可以看到,沿著平面上的 2 個鍵觀察環戊烷,其中非平面碳原子最靠近我們,可以看到鍵的彎曲使氫原子能夠稍微脫離重疊,從而在一定程度上減輕了扭轉張力。
環己烷是最小的環,能夠具有 109.5° 的鍵角並保持交錯構象,使其沒有張力。
環己烷有 3 種主要構象,即椅式、反椅式和船式。椅式構象沒有鍵角張力、扭轉張力或空間張力。然而,船式構象確實具有空間張力,因為船式前後的高點處的氫原子略微重疊。
待辦事項
環己烷的不同構象在某些反應中會表現出不同的反應性。例如,E2 消除反應,我們將在本書的後面部分討論,需要鹵素原子和氫原子位於相鄰的碳原子且彼此共面,或 180°(反式)。在具有多個取代基連線到其碳原子的環己烷中,氫原子和鹵素原子可能位於相鄰的碳原子,但永遠不會共面,因此阻止反應發生。
在其他反應中,相鄰取代基的空間位阻,例如相鄰碳原子上的較大烷基,會阻止親核試劑攻擊所需的位點。出於這些以及其他原因,瞭解反應物的三維幾何形狀和結構以及正在發生的反應機理非常重要。
待辦事項
在某些化合物中,兩個或多個環融合在同一個分子中。這可能發生在脂肪族和芳香族化合物中。
如果兩個環在一個碳原子上相遇,並且該碳原子是兩個環的一部分,則該化合物被稱為螺環化合物。由於碳原子周圍四個配體的常規四面體鍵合,兩個環大致(但並非完全)彼此垂直。
如果兩個環在兩個或多個碳原子上橋接,則碳原子形成橋的一部分,並且該化合物是雙環烷烴(對於兩個環)或多環烷烴(對於三個或更多環)。
芳香族雙環化合物是萘 (C10H8),它是由兩個苯環融合在碳-碳鍵上形成的。脂肪族(非芳香族)雙環化合物是十氫萘 (C10H18),正式名稱為十氫萘,它是由兩個環己烷環融合在 C-C 鍵上形成的。
雙環烷烴環系統由三個部分組成
- 較長的碳鏈 (a)
- 較短的碳鏈 (b)
- 碳-碳橋 (c)
注意 始終成立。
雙環環的命名方式如下,根據碳的總數進行命名
- 雙環[a.b.c]烷
在此公式中,將 [a.b.c] 替換為碳鏈的長度,並將“烷”替換為碳的總數(庚烷、辛烷、壬烷等)。
一個著名的雙環化合物例子是降冰片烷(見下圖)。降冰片烷的正式名稱是雙環[2.2.1]庚烷。橋的左側有兩個碳,橋的右側有兩個碳,橋本身有一個碳。因此,括號中的數字為 [2.2.1]。請注意,橋底部的兩個碳沒有計入括號中。
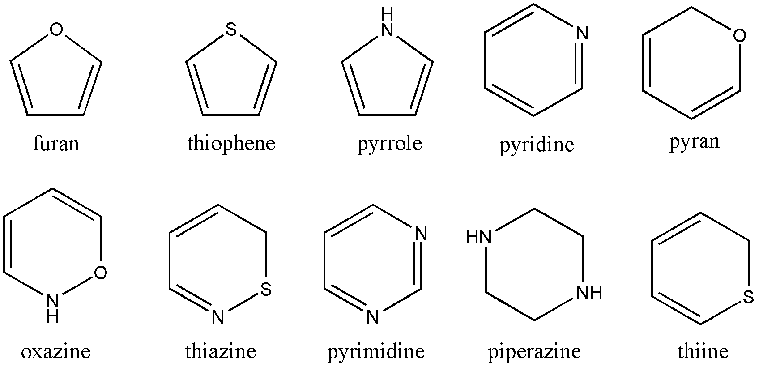
雜環化合物是指環中包含碳以外的原子的環狀化合物。上圖僅顯示了一些單環雜環化合物。所示的只是 5 元和 6 元環。還有更小和更大的環,以及多環雜環。
雜環化合物在有機化學中起著重要作用,由於它們的電子構型與碳不同,因此它們的反應方式不同於碳環,並且彼此之間也不同。在本書的後面,我們將討論幾種在有機化學中非常常用的特定雜環化合物,並討論它們的各自特性。
現在,重要的是要知道什麼是雜環化合物。


