結構生物化學/有機化學/有機官能團/羥基
羥基是有機化學中研究的眾多官能團之一。羥基的存在表明該分子要麼是醇要麼是羧酸。羥基的化學表示為–OH,表示氧原子共價鍵合到氫原子。
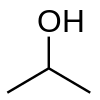
在醇的一般官能團中,有三個亞組:伯醇、仲醇和叔醇。醇根據它所連線的碳原子進行分類,伯醇、仲醇或叔醇。如果醇連線到只有一個碳-碳鍵的碳原子,則該醇為伯醇。同樣地,如果醇連線的碳原子與另外兩個碳原子相連,則該醇為仲醇,如果碳原子剩餘的三個鍵與其他碳原子相連,則該醇為叔醇。以下分別是伯醇、仲醇和叔醇的例子:乙醇、異丙醇(IUPAC 命名法:丙-2-醇)和叔丁醇(IUPAC 命名法:2-甲基丙-2-醇)。
 |
 |
氧和氫之間存在的鍵明顯短於碳和氫之間形成的鍵。羥基本質上是極性的。共價鍵中的氧原子具有很高的電負性;因此,它將共價鍵中共享的大部分電子密度拉向自身。從這些資訊可以清楚地看出,氧原子帶有明顯的負偏電荷,而氫原子則帶有相同大小的正偏電荷。
極性基團的存在使得醇能夠與其他分子形成氫鍵。例如,在乙醇中,一個乙醇分子上的帶負電的氧原子被吸引到另一個乙醇分子上的帶正電的氫分子。醇之間能夠形成氫鍵解釋了它們的熔點較高。醇的沸點也高於含有相當數量碳原子的烴類和醚類。
醇在水中的溶解度很有趣,因為醇具有疏水和親水中心,使其成為兩親性物質或兩親性物質。醇的烴部分是非極性的,因此抵抗在水中的溶解;極性醇基團是親水的,因此促進在水中的溶解。在丙醇這樣的小分子中,醇會溶解,因為極性醇基團的重量超過了非常短的氫鏈。然而,隨著烴鏈從丁醇增加到戊醇和己醇,醇在水中的溶解度變得幾乎不可混溶。
醇是兩性物質,既可以作為酸也可以作為鹼存在。在低 pH 值或被強酸包圍時,它們可以被質子化成烷氧鎓離子。相反,在高 pH 值下,以及被強鹼包圍時,它們可以以烷氧負離子形式存在。
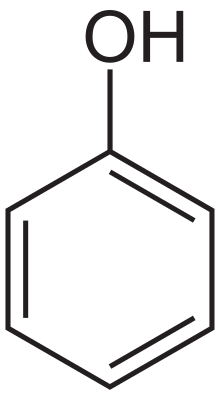
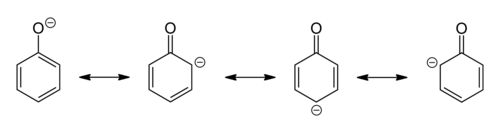
酚是羥基芳烴。它們在氧原子的化學反應性方面與醇有一些相似之處,但它們的酸性更強,鹼性更弱。它們似乎是烯醇(羥基連線到烯烴上)並且應該比酮式不穩定,但芳香性的增加使它們處於烯醇式比酮式更穩定。對共振形式的檢查表明,羥基將電子密度捐獻給環,因此羥基是活化基團,並且是鄰位-對位定位基團。 
取代酚被命名為母體化合物苯酚的衍生物,其中帶有羥基的碳原子被指定為 C-1。一些例子是
| 2-甲基-4,6-二硝基苯酚 | 苯-1,3-二醇 |
|---|---|
 |

|
酚的 pKa 值約為 8-10。酚的酸性比醇強得多。這是因為苯酚負離子(相應的共軛鹼)是共振穩定的。
無法直接協同取代芳香環上的離去基團。在適當取代的環中,離去基團可以透過親核過程透過兩步機制被羥基取代:親核芳香取代反應。
酚會發生與醇相同的許多反應,特別是在涉及相應苯酚負離子(烷氧負離子)的親核性時。
在工業上,甲醇是以數十億磅的規模從稱為合成氣的 CO 和 H2 的加壓混合物中製成的。該反應涉及由銅、氧化鋅和氧化鉻 (III) 組成的催化劑。
將催化劑改為銠或釕會導致 1,2-乙二醇(乙二醇)的生成,這是一種重要的工業化學品,是汽車防凍劑的主要成分。乙醇透過糖的發酵或透過磷酸催化的乙烯(乙烯)水合反應以大量製備。
在比工業規模小的範圍內,我們可以從各種各樣的起始原料製備醇。例如,透過特徵性地使用氫氧化物和水的 Sn2 和 Sn1 過程,將滷代烷轉化為醇。然而,這些方法的使用並不像人們想象的那樣廣泛,因為所需的滷代烷通常只能從相應的醇中獲得。它們還存在親核取代反應的通常缺點:在受阻體系中,雙分子消除反應可能成為主要的副反應,而叔滷代烷會形成可能發生 E1 反應的碳正離子。一些這些缺點透過使用極性非質子溶劑來克服。
從概念上講,減少羰基的最簡單方法是直接在碳氧雙鍵上新增氫,H-H。雖然可以做到這一點,但這需要高壓和特殊的催化劑。更方便的方法是極性過程,其中氫負離子和質子同時或依次傳遞到雙鍵。
有機金屬試劑
[edit | edit source]鎂和鋰的有機金屬試劑用於合成醇。由於有機金屬化合物中的金屬極具正電性,碳可以表現出帶負電荷的反應(賦予其親核行為)。這些有機金屬化合物可以攻擊醛和酮的羰基。該反應的一個重要特徵是在該過程中形成了新的碳碳鍵。[1]

該反應的第一步涉及親核碳攻擊酮或醛的羰基碳以形成碳碳鍵。同時,來自碳氧雙鍵(羰基)的兩個電子被來自攻擊碳的電子推開,形成金屬醇鹽與有機金屬化合物中的金屬。經過水性處理後,透過水解金屬醇鹽形成醇。[1]
透過改變與有機金屬化合物反應的化合物,可以形成不同型別的醇。例如,有機金屬化合物與甲醛的反應將生成伯醇。與任何其他型別的醛的反應將生成仲醇;與酮的反應將生成叔醇。[1]
羥基化
[edit | edit source]代謝降解的一個重要功能是在我們身體中未功能化的分子部分引入羥基(羥基化)。一組被稱為細胞色素蛋白的蛋白質是幾乎所有活細胞中都存在的至關重要的生物分子,它們幫助羥基化過程。細胞色素 P-450 是細胞色素蛋白的一個例子。細胞色素 P-450 使用 O2 將羥基新增到烷基取代基中。羥基化的重要性可以透過排洩藥物來防止毒性積累來體現。羥基化透過在化合物的特定區域新增羥基來幫助提高化合物的水溶性。因此,在肝臟中,羥基化有助於透過使其更易溶來加速我們攝入的藥物的排洩。如果沒有這個過程,攝入的藥物會停留在我們體內的更長時間,並且有更大的機會積累毒性。 [1]
羥基化在將羥基新增到分子中也具有選擇性。經歷羥基化的蛋白質可以控制羥基新增的順序,以及新增的位置。這是羥基化過程的關鍵功能,因為它允許分子在分子的特定區域發生氧化。它還允許分子以特定的方向與其他化合物結合或反應。 [1]
命名法
[edit | edit source]用於命名有機分子的系統 - IUPAC - 對醇來說相對容易使用,但如果含有醇基的分子包含含有其他官能團的取代基,例如烯烴、炔烴或鹵素,則會變得更加複雜。最簡單的情況是分子僅包含烴,羥基是唯一的官能團,使其純粹為醇。
一般來說,官能團的存在由一個特徵字尾表示,該字尾對每個官能團都是不同的,以及一個指定官能團在分子上的位置的數字。對於醇,使用的特徵字尾是 -ol。
情況 1:烴和醇在這種情況下,烴的最長鏈被計數 - 這成為分子中主要烴鏈。然後對最長的碳鏈進行編號,目的是在羥基上放置儘可能小的數字。最長的鏈按烷烴的命名方式命名,但醇的字尾是 -ol。因此,含有在第二個碳上含有醇基的丙烷鏈被命名為丙-2-醇或 2-丙醇。由於醇是唯一的官能團,所以使用這兩個名稱中的哪一個並不重要。假設“2”對應於羥基的位置。但是,當存在其他官能團時,此規則並不總是成立。
情況 2:這更復雜,因為在有機化學中存在官能團的等級。每個官能團在孤立時都希望被標記為最小的數字。但是,一些官能團具有“更重要的意義”,因此首先被編號。此外,如果醇不再是最“重要的”官能團,則該分子不具有醇的字尾。這在最初可能會出現一個小問題,因為 -ol 是該分子具有 -OH 基團的唯一提示。但是,-OH 基團的存在透過在與 -OH 基團鍵合的碳的數字之後使用“羥基”一詞來表示。例如:1-氯-2-羥基苯。
如果存在多個 -OH 基團,則命名法僅略有修改。名稱中使用的字尾是醇基數目,後跟 -ol。例如,含有兩個 -OH 基團的化合物具有“二醇”字尾;對於含有三個 -OH 基團的化合物,字尾是“三醇”。包含醇基的碳的數字以與只有一個醇基相同的方式表示;使羥基具有儘可能低的數字。例如,二醇將被命名為 3,3 戊二醇。此名稱表明五碳鏈中的第三個碳與兩個 -OH 基團鍵合。
醇和酚的獨特紅外光譜
[edit | edit source]紅外光譜是化學家用來闡明有機化合物結構資訊的技巧。有機分子在紅外區域吸收電磁輻射並促進特定的振動狀態。這些振動被稱為基頻吸收,它們是由從基態激發到最低能量激發態引起的。這些振動模式然後被機器拾取,該機器以光譜的形式解釋輻射。由於每種型別的共價鍵具有不同的自然振動頻率,因此兩種不同的分子永遠不會共享相同的光譜。某些鍵的吸收具有非常獨特的振動頻率。一小部分吸收可以分配給特定型別的鍵。例如,大約 1715 的吸收通常是由於羰基引起的。
醇和酚具有獨特的紅外光譜,通常在 3400 和 3300 cm−1 之間顯示出強而寬的拉伸帶。在溶液中,有時可以觀察到大約 3600−1 處有一個自由拉伸帶,具有尖銳但較弱的峰。
眾所周知的醇或酚峰是由 O-H 之間的拉伸振動產生的。分子間氫鍵通常會削弱 O-H 鍵,並將該帶移到較低的頻率。已知酚比醇具有更寬的 O-H 帶。然而,由於它們的形狀相似,很難透過觀察 O-H 帶來確定差異。C-O-H 之間的彎曲振動通常在 1440–1220 cm−1 處產生弱而寬的峰。然而,這些峰由於強 CH3 彎曲峰的類似帶的干擾而難以看到。從 1260 – 1000 cm−1 觀察到強烈的 C-O 鍵拉伸。由於 C-O 鍵與 C-C 鍵相鄰,因此峰的形狀和大小可用於確定醇是伯醇、仲醇還是叔醇。它還可用於區分酚和醇。此外,在醯胺、醚和醛中存在的醇也可以在紅外光譜中區分。紅外光譜是一種有用的分析工具,用於識別哪些官能團存在或哪些官能團不存在。
醇基的核磁共振
[edit | edit source]核磁共振 (NMR) 是一種用於識別有機化合物的技術。由於原子核由於帶正電的質子而具有自旋電荷,因此它可以產生磁場。正因為如此,質子將具有兩種方向,即 β 和 α 自旋態,它們在存在外部磁場的情況下具有不同的能量。當化合物暴露於電磁輻射時,會發生共振(當原子核在方向之間來回翻轉時),當輻射量與兩種自旋態的能量差相匹配時,會記錄 NMR 訊號,NMR 檢測器會記錄峰。
核磁共振 (NMR) 最常見的形式之一是質子核磁共振 (H+ NMR)。NMR 譜圖透過不同基團的化學位移來解讀。在質子 NMR 中,含有 -OH 基團的化合物在約 0.5-5.0 ppm 處會有化學位移(峰)。例如,乙醇在約 4.0 ppm 處會有一個峰,表示羥基,而其在約 1.0 ppm 和約 3.0 ppm 處的另外兩個峰則表示 C-H 質子的位置,這與它們在化合物中的位置有關。
1. Schore, Neil E. (2011). 有機化學結構與功能 第 6 版. W. H. Freeman.
2. Hammond, Christina N., Mohrig, Jerry R., Schatz, Paul F.. (2010). 有機化學實驗技術 第 3 版. W.H. Freeman.
3. Atkins, Peter, Jones, Loretta. (2008). 化學原理:探索洞察 第 4 版. W. H. Freeman.