結構生物化學/化學鍵/氫鍵
氫鍵是由偶極-偶極力形成的,這種力存在於一個電負性原子(氫鍵受體)和一個與另一個相同分子或不同分子的電負性原子(氫鍵供體)共價結合的氫原子之間。只有氮、氧和氟原子可以與氫相互作用形成氫鍵供體;這與氫共價鍵不同。然而,氫鍵受體可以是任何參與極性鍵、具有電負性和具有孤對電子的原子。在氫鍵中,氧、氮或氟上的孤對電子與共價鍵合到這些原子之一的部分正電荷的氫相互作用。氫鍵中的氫原子由兩個電負性原子(如氧或氮)共享。)氫鍵負責DNA雙螺旋結構中特定的鹼基配對,並且是DNA雙螺旋結構穩定性的主要因素。氫鍵供體包括氫原子和與其最緊密結合的原子。氫鍵在蛋白質的結構中也起著非常重要的作用,因為它穩定了由α螺旋、β摺疊、轉角和環形成的蛋白質的二級、三級和四級結構。氫鍵連線了蛋白質結構中不同多肽鏈之間的氨基酸。氫鍵受體是與氫原子結合較弱的原子。
氫鍵從根本上說是靜電相互作用,並且比共價鍵弱得多。然而,它們是最強型別的偶極-偶極相互作用。氫原子所鍵合的電負性原子會將電子密度從氫原子處拉走,從而產生部分正電荷。因此,氫原子可以透過靜電相互作用與部分帶負電的原子相互作用。

氫鍵是靜電相互作用的一種形式,發生在與兩個電負性原子鍵合的氫原子之間;其中一個是氫鍵供體,在其自身與氫之間具有更強的鍵。這些電負性原子是氮、氧和氟;這種電負性原子會將電子密度從氫原子處拉走,使其帶部分正電荷。這種部分正電荷被氫鍵受體(富電子密度原子)的部分負電荷吸引。氫鍵供體、氫原子和氫鍵受體之間形成的化學鍵具有直線形結構。
氫鍵(H鍵)是分子之間或分子內部的非共價鍵合型別,可以是分子間或分子內的。這種鍵合型別比共價鍵和離子鍵弱得多且長得多,但比範德華相互作用強。它也具有一些共價鍵的特點:直接且筆直。換句話說,H鍵供體和H鍵受體位於一條直線上。為了形成H鍵,需要H鍵供體和H鍵受體。H鍵供體是指其氫原子與具有可用價電子的高電負性小原子鍵合的分子(N、F和O最符合上述描述,因為它們非常電負性,使得與其共價結合的H非常正)。H-O、H-N和H-F鍵極性非常強;因此,電子密度很容易從氫原子處被拉向電負性原子。一個分子中的部分正電荷氫被另一個分子上電負性原子的部分負電荷孤對電子吸引,並且由於這種相互作用,H鍵形成。所有氫鍵的強度都各不相同。
關於氫鍵的其他重要事實如下。氮、氧和氟的小尺寸對於氫鍵至關重要,原因有兩個。一個是它使這些原子具有電負性,使其共價鍵合的H高度為正。另一個原因是它允許另一個氧、氮或氟上的孤對電子靠近H。此外,氫鍵在許多系統中具有深遠的影響。氫鍵也參與了許多酶的作用[物質和變化的分子性質]。
氨、水和氟化氫的沸點都高於其他類似的分子,這是由於氫鍵造成的。氫與這些強電負性原子之間的鍵極性很強,氫上帶部分正電荷。這種部分正電荷氫強烈地被相鄰分子上部分負電荷的氧吸引。一般來說,沸點隨著分子量的增加而升高,這是因為額外的質量需要更高的溫度才能使分子快速運動,並且因為較重的分子具有更大的倫敦力。水的凝固點也比其他類似的分子高得多。一個不尋常的特點是,當它凍結時,密度會降低。每個氧原子周圍的四面體結構,有兩個規則的氫鍵和兩個與其他分子的鍵。這需要冰分子之間有很大的空間。籠形水合物是捕獲在固體(如冰)孔洞中的分子,理論上可以被用作麻醉劑。
氫鍵對分子的沸點有顯著影響。沸點通常隨著摩爾質量的增加而增加。然而,參與分子間氫鍵鍵合的分子與摩爾質量相同但不參與氫鍵鍵合的分子相比,具有更高的沸點。這是因為異常強的氫鍵力允許水分子之間發生更強的相互作用,從而形成更強的鍵和更高的沸點。[1]此外,氫鍵是造成水的許多異常性質的原因,例如其高沸點、熔點、汽化熱、高介電常數、表面張力、毛細作用等。
氫鍵可以在氫和另外四種元素之間發生。氧(最常見)、氟、氮和碳。碳是一種特殊情況,只有當它與非常電負性的元素(如氟和氯)結合時,它才會真正參與氫鍵。[1]
氫鍵是生物化學中三種主要大分子(如蛋白質、核酸和碳水化合物)的重要組成部分。氫鍵負責蛋白質(酶)的結構和性質。由於存在官能團,氫鍵適用於這些生物分子。其中一些是羧酸、醇甚至胺基團。它們可以提供氫、氧或氮用於可能的氫鍵。[1]

如前所述,氫鍵可以是分子間的(例如,水分子之間的鍵合),也可以是分子內的(例如,蛋白質和DNA的鍵合)。蛋白質的二級結構是由氨基酸之間的氫鍵形成的。例如,α-螺旋是一種棒狀的二級結構,它是由於(i)個氨基酸的羧基與(i+4)個氨基酸的氨基之間形成氫鍵而產生的。轉角(環家族)是一種二級結構,它是由(i)個氨基酸的羧基與(i+3)個氨基酸的氨基之間形成氫鍵而產生的。β-摺疊是一種二級結構,它是由兩個或多個β-鏈之間的氫鍵形成的。反平行β-鍊形成的氫鍵是直的,因為羰基和氨基直接對齊,而平行β-鍊形成的氫鍵則略微弱一些,因為羰基和氨基沒有完美對齊,從而形成更長且更弱的氫鍵。
蛋白質在水中的溶解度取決於其與蛋白質表面形成氫鍵的能力。具有更大親水錶面含量的蛋白質通常更能夠與周圍的水形成氫鍵。溶液鹽濃度的改變,如在鹽析/鹽溶中進行的那樣,會產生一種遮蔽效應,從而降低了與水中氫形成氫鍵的能力。鹽析蛋白質沉澱法在蛋白質分離中利用了這一概念。

氫鍵最簡單的例子可以在水分子中找到。水分子由一個氧原子連線到兩個氫原子組成。兩個水分子之間可以形成氫鍵。在存在許多水分子液態水中,每個水分子都可能與多達4個其他分子形成氫鍵(2個透過其2個氫原子,每個氫原子與另一個氧原子形成氫鍵,另外2個透過其氧原子上的2個孤對電子,可以與另外2個氫原子形成氫鍵)。
儘管水分子量低,但它具有異常高的沸點。這種特性可以歸因於水內部存在大量的氫鍵。由於這些鍵難以斷裂,因此與其他類似但缺乏氫鍵的液體相比,水的熔點、粘度和沸點都相對較高。與某些也具有氫鍵的其他液體相比,水包含大量氫鍵(最多4個)。一個例子是氨,其中氮只有一個孤對電子但有3個氫原子,因此最多隻能形成2個氫鍵。
氫鍵還可以解釋為什麼冰的密度小於液態水的密度。在水的液態形式中,使分子緊密結合在一起的氫鍵在室溫下不斷斷裂和重新形成。但當水變成冰時,氫鍵導致水分子形成剛性晶格結構,這會導致分子之間出現較大的間隙,從而導致其密度較小但體積較大。
氫鍵也解釋了水的表面張力高的原因。水分子之間大量氫鍵的可用性(每個水分子有4個氫鍵)證明了它們彼此粘附得多麼好,形成了一個強大而有彈性的表面。可以觀察到此特性的常見示例包括一個裝滿超過頂部但沒有溢位的杯子,或者能夠停留在水上而不破壞其表面的小型生物。
水根據溫度的不同具有不同數量的氫鍵。據估計,在0°C時,每個水分子平均具有3.69個氫鍵,而在25°C時,它平均具有3.59個氫鍵,而在100°C時,它平均具有3.24個氫鍵。隨著溫度升高,氫鍵減少,這可以歸因於分子運動的增加。
DNA包含四個鹼基:鳥嘌呤、胞嘧啶、腺嘌呤和胸腺嘧啶。鳥嘌呤與胞嘧啶和腺嘌呤與胸腺嘧啶的互補鹼基對利用氫鍵相互連線。這些互補核苷酸之間的氫鍵使DNA雙螺旋的兩個鏈保持在一起。每個鹼基還可以與外部環境(例如水)形成氫鍵。儘管這些內部和外部氫鍵相當弱,但DNA中所有數百萬個氫鍵的綜合力量使其成為一個穩定的分子。此外,每個核苷酸上磷酸基團上的氫鍵相互作用,導致兩條DNA鍊形成螺旋結構。
DNA中的鹼基配對(一個嘌呤和一個嘧啶鹼基)可以更詳細地解釋。除了將DNA鏈連線在一起外,互補鹼基之間的氫鍵還將鹼基隔離在雙螺旋的內部。因此,鹼基之間的氫鍵增強了穩定DNA的疏水作用。疏水鹼基再次保留在螺旋的內部,而極性外部則接觸溶劑水。氫鍵是一種弱的分子力,但它是一種穩定DNA分子的累加效應。鹼基透過氫鍵精確地結合在一起,能量為1至5 kcal/mol(4至21 kJ/mol)。
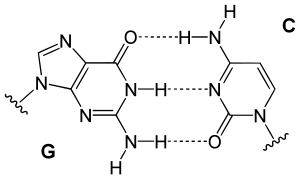
一個嘌呤(鳥嘌呤和腺嘌呤)和一個嘧啶(胞嘧啶和胸腺嘧啶)的DNA鹼基中的氫鍵 tạo ra hình dạng tương tự。鳥嘌呤和胞嘧啶配對的形狀和結構與腺嘌呤和胸腺嘧啶配對的形狀和結構非常相似。胞嘧啶和鳥嘌呤透過三個氫鍵結合在一起。腺嘌呤和胸腺嘧啶配對共享兩個氫鍵,因此鍵略微弱一些且略長一些。
 |
 |
Silberberg, Martin S. 化學“物質和變化的分子本質”。第五版。2009年。
Berg,Jeremy;Tymoczko,John;Stryer,Lubert。生物化學,第6版。W.H. Freeman and Company。2007年。(8) https://wikibook.tw/wiki/Structural_Biochemistry/Chemical_Bonding/Dipole_interaction https://wikibook.tw/wiki/Structural_Biochemistry/Nucleic_Acid/DNA https://wikibook.tw/wiki/Structural_Biochemistry/Chemical_Bonding/Covalent_bonds https://wikibook.tw/wiki/Structural_Biochemistry/Proteins https://wikibook.tw/wiki/Structural_Biochemistry/Nucleic_Acid https://wikibook.tw/wiki/Structural_Biochemistry/Carbohydrates https://wikibook.tw/wiki/Structural_Biochemistry/Proteins/Structures https://wikibook.tw/wiki/Structural_Biochemistry/Proteins/Amino_Acids https://wikibook.tw/wiki/Structural_Biochemistry/Nucleic_Acid/Nitrogenous_Bases/Purines/Guanine https://wikibook.tw/wiki/Structural_Biochemistry/Nucleic_Acid/Nitrogenous_Bases/Purines/Cytosine https://wikibook.tw/wiki/Structural_Biochemistry/Nucleic_Acid/Nitrogenous_Bases/Purines/Adenine https://wikibook.tw/wiki/Structural_Biochemistry/Nucleic_Acid/Nitrogenous_Bases/Purines/Thymine https://wikibook.tw/wiki/Structural_Biochemistry/Water
