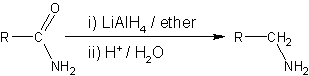結構生物化學/有機化學/有機官能團/氨基

氨基由一個與兩個氫原子鍵合的氮原子組成。氨基可以作為鹼,因為它們可以從溶液中吸收一個 H+。氨基可以在鹼性條件下以 1+ 的電荷被電離。含有氨基的有機化合物被稱為“胺”;含有氨基和羧基的有機化合物被稱為氨基酸,它們是蛋白質的組成部分。
胺可以很容易地形成氫鍵。DNA鹼基中的胺與附近的氮或氧原子形成氫鍵,並將兩條鏈連線在一起。
例如,賴氨酸[[|]] 的氨基已被證明在基因調控中非常有用。特別是在組蛋白中賴氨酸的氨基被乙醯化時,它就無法像平時一樣發揮作用。這是參與基因表達和複製的一個調節步驟。
氨基在生物化學中的另一個作用是酶。在蛋白酶的情況下,一種切割氨基酸的酶,當絲氨醇的羥基攻擊氨基酸的羰基碳時,就會形成四面體過渡態。由於四面體過渡態帶負電荷,正的 NH3+ 電荷有助於穩定過渡態,形成所謂的氧陰離子環。
胺由於其孤對電子也可以作為親核試劑。這是肽鍵形成的基礎,其中羰基碳在脫水反應中充當親電試劑。

胺氮為 sp3 雜化,呈四面體形狀。氮的非鍵合對電子就像一個取代基——氮周圍的幾何形狀是四面體,鍵角都大約為 109°。與碳不同,sp3 雜化的氮不穩定,在室溫下會發生快速翻轉。它類似於雨傘從裡到外翻轉,類似於 SN2 反應中發生的構型翻轉。
遵循所有常用的 IUPAC 規則。在名稱末尾新增字尾 –胺,並指定氨基的位置。對於 2° 和 3° 胺,選擇最大的烷基取代基作為母體,氮上的其他烷基以 N- 作為字首命名,表示它們連線到氮上。由於胺官能團在命名中優先順序最低,因此它通常被命名為更具功能性分子的取代基。
胺的酸性遠低於醇,pKa 約為 35,Keq = 10-35。必須使用非常強的鹼,例如烷基鋰,才能完全去質子化胺。
胺是常見的有機官能團中最鹼性的,但仍然是相當弱的鹼。質子化僅發生在非鍵合電子對上。胺的鹼性直接取決於氮原子上的“電子密度”。感應效應和共振效應都可以改變氮原子的鹼性。
N 上的雜化也會影響鹼性。原子上的 s 特徵增加會增加該原子的電負性,這有利於酸性,因此不利於鹼性。因此,sp3 雜化的氮比 sp2 或 sp 雜化的氮更鹼性。

1. 氰化物取代烷基鹵化物,然後還原
2. LiAlH4 還原醯胺
3. 用疊氮化物取代,然後還原
4. Gabriel 合成 1° 胺
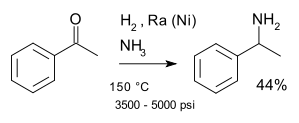
5. 還原胺化
伯胺將在 3200 cm-1 – 3500 cm-1 處給出兩個短而尖的相同峰
仲胺將在 3320 cm-1 處給出單個短而尖的峰
叔胺在任何區域都不會給出峰。
1. http://orgchem.colorado.edu/Spectroscopy/irtutor/aminesir.html